(14分)化学反应原理在科研和工农业生产中有广泛应用。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g)  2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示: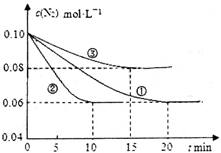
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=__________________;与实验①相比,实验②和实验③所改变的实验条件分别为下列选项中的__________、__________(填字母编号)。
A.增大压强
B.减小压强
C.升高温度
D.降低温度
E.使用催化剂
(2)已知NO2与N2O4可以相互转化:2NO2(g) N2O4(g)。
N2O4(g)。
①T℃时,将0.40 mol NO2气体充入容积为2L的密闭容器中,达到平衡后,测得容器中c(N2O4)="0.05" mol/L,则该反应的平衡常数K=_______________;
②已知N2O4在较高温度下难以稳定存在,易转化为NO2,若升高温度,上述反应的平衡常数K将_____________(填“增大”、“减小”或“不变”)。
③向绝热密闭容器中通入一定量的NO2,某时间段内正反应速率随时问的变化如图所示。下列说法正确的是__________(填字母编号)。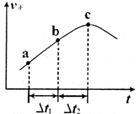
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.Δt1=Δt2时,NO2的转化率:a~b段小于 b~c段
(3)25℃时,将amol/L的氨水与b mol/L盐酸等体积混合,反应后溶液恰好显中性,则a______b。 (填“>”、“<”或“=”);用a、b表示NH3 H2O的电离平衡常数Kb=________________。
H2O的电离平衡常数Kb=________________。
(6分)已知A、B、C、D四种短周期元素在元素周期表中的相对位置如下图所示,它们的原子序数之和为46。
请填空:
(1)C元素的元素符号为______________________________
D元素的原子结构示意图____________________________
(2)B元素氢化物的电子式____________________________________
(3)A元素可以形成多种同素异形体,其中硬度最大,不导电的是________________(填物质的名称),它属于_____________晶体;熔点高,可以导电的是_____________(填物质的名称)。
(8分) 在室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适反应条件下,它们可以按下列框图进行反应。又知E溶液是无色溶液。请回答:
(1) (用化学式填空)
A是______________B是________________
(2)反应①的化学方程式为___________________________________________
反应③的离子方程式为___________________________________________
反应⑤的化学方程式为___________________________________________________
(12分)根据要求回答相关问题:
(1) 除去下列物质中所混有的少量杂质(括号内为杂质),写出有关的反应方程式。
①铜粉 (铝粉) ;
②FeCl3溶液(FeCl2 );
③N2 (O2) ____________________________________________________。
(2)下图所示各项变化的未知数中均含有钠元素,E为淡黄色粉末,据此回答下列问题:
①写出A→B的化学方程式,标出电子转移的方向和数目;
____________________________________________________________
②在B→C的变化中所得C的溶液往往不纯,其中的杂质(不包括水)可能是,主要原因是;还可能是,主要原因是。
(8分)某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等离子,进行如下实验:
(1)加入过量的稀盐酸,有白色沉淀生成。
(2)过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
(3)过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现。
(4)另取少量步骤(3)中的滤液,加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:待测液中一定含有离子;
一定不含有离子;还有_________________离子不能确定是否存在,要检验这些离子的实验方法是,操作是______________________________________________。
有一已磨成粉末的混合物试样,是由下列六种物质中的若干种等量组成﹕
(A) NaCl (B) KCl (C) CaCl2 (D) CuSO4( 无水) (E) Na2SO4 (F) Na2CO3
为了要确定该粉末试样的成分,某研究性学习小组先查了资料后,研拟了一个检验粉末试样的流程图,并在老师的指导下在化学实验室中进行实验。以下是该小组实验报告的一部份:
实验一:用烧杯取粉末试样约2g,加蒸馏水约100mL,搅拌后形成无色的透明溶液X。
实验二:在溶液X中加了盐酸,观察到在溶液中陆续产生气泡,至溶液不再冒气泡,溶液仍为无色透明(贴上卷标Y)。
实验三:在无色透明的溶液Y中,滴加BaCl2溶液,即见白色沉淀。
实验四:继续滴加BaCl2溶液,至白色沉淀不再产生后,过滤分离出白色沉淀,得到透明的无色滤液Z。
实验五:在滤液Z中,滴入AgNO3溶液,则见白色沉淀,加入稀硝酸,沉淀不溶解。
(1)根据上述实验报告,原粉末中一定没有哪两种物质﹖(从(A) -(F)中选两项,填字母)
(2)原粉末中,一定含有哪两种物质﹖(从(A) -(F)中选两项)
(3)若只需回答上述(1)(2)的问题,你认为该小组同学不需要做哪两个实
验
(A) 实验一 (B) 实验二 (C) 实验三 (D) 实验四 (E) 实验五