下列离子方程式书写正确的是
| A.NaHSO4溶液与Ba(OH)2溶液反应至中性: H++SO42-+Ba2++OH- = BaSO4↓+H2O |
| B.钢铁发生吸氧腐蚀的正极反应式:O 2+ 4e-+2H2O=4OH— |
| C.足量的溴化亚铁和少量的氯气反应:2Fe2++4Br-+3Cl2=3Fe3++2Br2+6Cl- |
D.用铁作电极电解饱和食盐水:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
下列关于有机物的说法正确的是()
| A.乙醇、乙烷和乙酸都可以与钠反应生成氢气 |
| B.75%(体积分数)的乙醇溶液常用于医疗消毒 |
| C.苯和乙烯都可使溴的四氯化碳溶液褪色 |
D.石油分馏 可获得乙酸、苯及其衍生物 可获得乙酸、苯及其衍生物 |
2007年3月温家宝总理在十届全国人大五次会议上提出“要大力抓好节能降耗、保护环境”,下列举措中违背了这一指导思想的是()
| A.加大开发太阳能、水能、风能、地热能等能源力度,减少化石燃料的使用 |
B.研制乙醇汽油技术 ,降低机动车辆尾气中有害气体排放 ,降低机动车辆尾气中有害气体排放 |
| C.生产、生活中,努力实现资源的循环利用 |
| D.利用高新技术,提高石油、煤、天然气产量,以满足工业生产快速发展的需求 |
同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是()
| A.2Na218O2 + 2H2O = 4Nal8OH + O2↑ |
| B.2KMnO4 + 5H218O2 + 3H2SO4 = K2SO4 + 2MnSO4 + 518O2↑+ 8H2O |
C.NH4Cl + 2H2O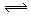 NH3·2H2O + HCl NH3·2H2O + HCl |
| D.K37ClO3 + 6HCl = K37Cl + 3Cl2↑+ 3H2O |
NA表示阿伏加德罗常数的 值,下列说法正确的是( )
值,下列说法正确的是( )
| A.5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
| B.1 mol Na2O2与足量H2O充分反应,转移的电子数为2NA |
| C.7.8gNa2O2中含有的阴离子数等于0.1NA |
| D.0.5mol雄黄(As4S4,结构如右图)含有NA个S—S键 |

下列说法中正确的是 ( )
| A.氯化钠水溶液在电流的作用下电离出Na+和Cl- |
| B.硫酸钡难溶于水,但硫酸钡属于强电解质 |
| C.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质 |
| D.硫酸钠在水中的电离方程式可表示为Na2SO4===2Na++S6++4O2- |