下图是模拟电化学反应装置图。下列说法正确的是
| A.若X为碳棒,开关K置于N处,会加快铁的腐蚀 |
| B.若X为锌,开关K置于N处,则X极上有黄绿色气体生成 |
| C.若X为碳棒,开关K置于M处,则铁电极的电极反应式为: Fe-3e- =Fe3+ |
| D.若X为锌,开关K置于M处,则总反应方程式为:2Zn+O2+2H2O=2Zn(OH)2 |
下列对物质性质的描述中属于分子晶体的是
| A.熔点是97.80℃,质软、导电,密度是0.97g/cm3 |
| B.常温常压下是液体,溶于水后能导电 |
| C.熔点极高,硬度极大,液态、固态时,均不能导电 |
| D.固态不能导电,熔点较高,但在熔融状态可以导电 |
热化学方程式C(s)+H2O(g)  CO(g)+H2(g)△H=+131.3kJ/mol表示
CO(g)+H2(g)△H=+131.3kJ/mol表示
| A.碳和水反应吸收131.3kJ能量 |
| B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量 |
| C.1mol固态碳和1mol水蒸气反应生成1mol一氧化碳气体和1mol氢气,并吸热131.3KJ 热量 |
| D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ |
某主族元素R的最高正价与最低负化合价的代数和为4,由此可以判断
| A.R一定是第四周期元素 |
| B.R一定是ⅣA族元素 |
| C.R的气态氢化物比同周期其他元素气态氢化物稳定 |
| D.R气态氢化物化学式为H2R |
X、Y、Z、W均为短周期元素,它们在周期表中相应位置如图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中错误的是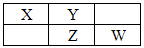
| A.Y的气态氢化物的稳定性较Z的强 |
| B.原子半径:W>Z>Y>X |
| C.W的最高价氧化物对应水化物的酸性较Z的强 |
| D.四种元素的单质中,Z的熔、沸点最高 |
下列各组物质中属于同分异构体的是
| A.H2O和D2O | B.O2和O3 |
| C.乙醇CH3CH2OH和二甲醚CH3-O-CH3 | D. 和 和 |