已知25 ℃时部分弱电解质的电离平衡常数数据如下表:
| 弱酸化学式 |
HSCN |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数 |
1.3×10-1 |
1.7×10-5 |
6.2×10-10 |
K1=4.3×10-7 K2=5.6×10-11 |
回答下列问题:
(1)写出碳酸的第一级电离平衡常数表达式:K1=_______________________。
(2)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为________(填字母)。
(3)常温下,0.1 mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 (填序号)
A.[H+] B.[H+]/[CH3COOH] C.[H+]·[OH-] D.[OH-]/[H+]
(4)25 ℃时,将20 mL 0.1 mol·L-1 CH3COOH溶液和20mL0.1 mol·L -1HSCN溶液分别与20 mL 0.1 mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是 反应结束后所得两溶液中,c(CH3COO-)________c(SCN-)(填“>”、“<”或“=”)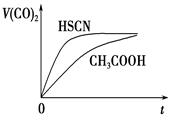
(5)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(6)25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=________mol·L-1(填精确值),
c(CH3COO-)/c(CH3COOH)=________。
(7)写出少量CO2通入次氯酸钠溶液中的离子方程式:_____________________________。
短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中B所处的周期序数与族序数相等。填写下列空白。
| A |
|||
| B |
C |
D |
(1)写出C的氧化物的一种用途:
(2)B单质与Fe2O3反应时,每消耗13.5g B时放热213kJ,该反应的热化学方程式是
(3)为防止A元素的氧化物AO2污染空气,科学家寻求合适的化合物G和催化剂,以实现反应:
AO2+X催化剂A2 +H2O+n Z(未配平,n可以为0)。上述反应式中的X不可能是(填标号)。
a.NH3b.COc.CH3CH2OH d.H2O2
(4)A元素的最简单氢化物甲、D元素的最高价氧化物对应的水化物乙都是很重要的基础化工原料。
①一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是(选填序号)。
| 选项 |
a |
b |
c |
d |
| x |
温度 |
温度 |
加入H2的物质的量 |
加入甲的物质的量 |
| y |
甲的物质的量 |
平衡常数K |
甲的转化率 |
生成物物质的量总和 |
②25℃时,往a mol·L-1的甲的水溶液中滴加0.01 mol·L-1乙溶液,当两种溶液等体积混合时,溶液呈中性(设温度不变)。滴加过程中溶液的导电能力(填“增强”、“减弱”或“不变”);
所得混合溶液中A、D两种元素的物质的量的关系为:A2D(填“大于”、“等于”或“小于”);甲中溶质的电离平衡常数Kb=(用含a的代数式表示)。
化合物I是工业上用途很广的一种有机物,实验室可以通过下列过程合成:
(1)A是一种气态烷烃,核磁共振氢谱只出现两组峰且峰面积之比为9:1,则A的分子式是______;
C的名称是______;
(2)B→C的反应条件是__________________;
(3)上述过程中属于消去反应的是______;(用字母→字母表示)
(4)H→I的化学方程式是________________________;
(5)G在浓硫酸存在下能生成多种化合物,写出符合下列条件的有机物的结构简式,含有六元环:_____;髙分子化合物:____________。
(6)I有多种同分异构体,其中与I具有相同官能团,不含支链且能发生银镜反应的有______种(不包括I,且不考虑立体异构),写出其中一种的结构简式:______。
氮、磷、锌是与生命活动密不可分的元素。请回答下列问题:
(1)NH3和pH3都是极性分子,其中极性较大的是______,理由是______。
(2)NH4NO3是一种重要的化学肥料,其中N原子的杂化方式是______。
(3)氮化硼(BN)的一种晶体结构与金刚石相似,则B-N-B之间的夹角是____________。氮化砸的密度为3.52g/cm3,则B-N键的键长是______pm (只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
(4)已知磷酸分子中,P、O原子均满足最外层8个电子的稳定结构,则:
①P与非羟基O之间的共价键的形成方式是____________;
②中和20mL0.1mol/L次磷酸(H3PO2)溶液需要0.1mo/L NaOH溶液的体积恰好为20 mL,则H3PO2的结构式是____________。
(5)Zn2+基态时的电子排布式是______,ZnO和ZnS的晶体结构相似,其中熔点较高的是______,理由是________________________
锰锌铁氧体可用于隐形飞机上吸收雷达波涂料。现以废旧锌锰电池为原料制备锰锌铁氧体的主要流程如下: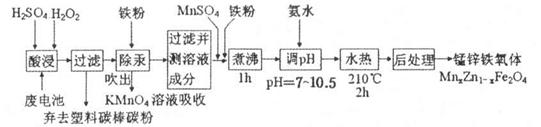
(1)酸浸时,二氧化锰被双氧水还原的化学方程式为_______。
(2)活性铁粉除汞时,铁粉的作用是______ (填“氧化剂”或“还原剂”或“吸附剂”)。
(3)除汞是以氮气为载气吹入滤液带出汞蒸汽经KMnO4溶液进行吸收而实现的。如下图是KMnO4溶液处于不同pH时对应的Hg去除率变化图,图中物质为Hg与 MnO4-在该pH范围内的主要产物。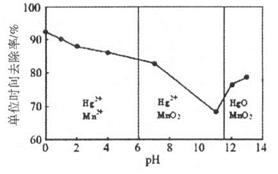
①请根据该图给出pH对汞去除率影响的变化规律:______。
②试猜想在强酸性环境下汞的单位时间去除率高的原因:______。
(4)当x=0.2时,所得到的锰锌铁氧体对雷达波的吸收能力特别强,试用氧化物的形式表示该铁氧体组成____________。
(5)经测定滤液成分后同时加入一定量的MnSO4和铁粉的目的是______。
I.科学家一直致力于“人工固氮”的方法研究。目前合成氨的技术原理为氮气和氢气在高温高压催化剂条件下生成氨气,一定条件下,向一个2L的密闭容器中充入2molN2和6molH2,反应达平衡时生成NH3的浓度为0.5mol/L,并放出QkJ热量,该反应的热化学方程式可表示为______。
II.已知:N2O4(g) 2NO2(g)△H=+57.20kJ/mol。
2NO2(g)△H=+57.20kJ/mol。
在1000C时,将0.100molN2O4气体充入lL恒容抽空的密闭容器中,每隔一定时间对该容器内的物质浓度进行分析得到下表数据:
| 时间(s) |
0 |
20 |
40 |
60 |
80 |
| c(N2O4)/mol |
0.100 |
c1 |
0.050 |
c3 |
c4 |
| c(NO2)/mol |
0.000 |
0.060 |
c2 |
0.120 |
0.120 |
(1)该反应的平衡常数表达式为______;从表中数据分析:c1______c2、c3______c4(选填“>”、“<”或“=”)。
(2)在右图中画出并标明此反应中N2O4和NO2的浓度随时间变化的曲线。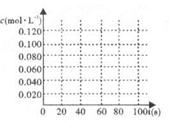
(3)在上述条件下,从反应开始至达到化学平衡时,四氧化二氮的平均反应速率为______。
(4)若起始时充入NO2气体0.200mol,则达到平衡时NO2气体的转化率为______;其它条件不变时,下列措施能提高NO2转化率的是______ (填字母)。
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度
D.升高温度E.再充入一定量的He
(5)向容积相同、温度分别为T1和T1的两个密闭容器中分别充入等量NO2,发生反应:2NO2 N2O4(g)(g)△H=-57.20kJ/mol。恒温恒容下反应相同时间后,分别测得体系中NO2的百分含量分别为a1和a2。巳知T1<T2,则a1____a2(选择A、B、C、D填空)。
N2O4(g)(g)△H=-57.20kJ/mol。恒温恒容下反应相同时间后,分别测得体系中NO2的百分含量分别为a1和a2。巳知T1<T2,则a1____a2(选择A、B、C、D填空)。
A.大于B.小于C.等于D.以上都有可能