下列离子方程式中,正确的是
| A.稀硫酸与氢氧化钡溶液反应:H+ +OH—=H2O |
| B.铁与氯化铁溶液反应:Fe +2Fe3+=3Fe2+ |
| C.实验室制氯气:MnO2+4HCl=Mn2++2Cl—+Cl2↑+2H2O |
| D.向氯化铝溶液滴加少量氨水:Al3++3OH—=Al(OH)3↓ |
下列叙述中正确的是( )
| A.同周期元素中,ⅦA族元素的原子半径原子大 |
| B.ⅥA族元素的原子,其半径越大,越容易得到电子 |
| C.室温时,零族元素的单质都是气体 |
| D.同一周期中,碱金属元素的第一电离能最大 |
下列表达方式错误的是( )
A.甲烷的电子式 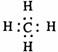 |
B.氟化钠的电子式  |
| C.硫离子的核外电子排布式 1s22s22p63s23p4 |
D.碳-12原子 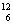 C C |
13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,Kurt Wuithrich等人为此获得2002年诺贝尔化学奖。下面有关13C、15N的叙述正确的是(
A.13C与15N有相同的中子数
B.13C电子排布式为1s22s22p3
C.15N与14N互为同位素
D.15N的电子排布式为1s22s22p4
若原子核外电子的排布的基本规律为最外层电子数不超过5个,次外层电子数不超过10个,倒数第三层电子数不超过15个,而各电子层电子的最大容量仍为2n2,则元素周期表中第三、第四、第五周期含有的元素分别有
| A.5种、10种、15种 | B.8种、18种、18种 |
| C.8种、10种、15种 | D.9种、10种、15种 |
某主族元素X的原子有一个未成对电子,其原子序数小于18,大于10,下列有关元素X的叙述正确的是( )
| A.一定是活泼金属元素 | B.一定是活泼非金属元素 |
| C.X的氧化物有两性 | D.X一定能形成离子化合物 |