在一些高档茶叶、点心等食品的包装盒中有一个小袋,将小袋打开,可以看到灰黑色粉末,其中有些已变成棕褐色。将上述粉末溶于稀盐酸,取上层清液,滴入几滴氯水,再滴加KSCN溶液,马上出现血红色。以下结论不正确的是
| A.该灰黑色粉末用作抗氧化剂 |
| B.该灰黑色粉末不可食用 |
| C.粉末变为棕褐色是因为与空气中的氧气作用 |
| D.该灰黑色粉末在起作用的过程中作为氧化剂 |
用1L1mol·L-1NaOH溶液吸收0.6molCO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为
| A.2︰3 | B.1︰2 | C.2︰1 | D.3︰2 |
14克铜、银合金与足量的某浓度的硝酸反应,将放出气体与1.12升(标况)氧气混合,通入水中恰好全部吸收,则合金中铜的质量是( )
| A.9.6克 | B.6.4克 | C.3.2克 | D.1.6克 |
将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法不正确的是()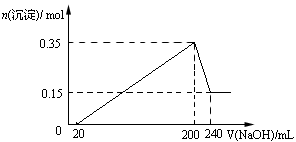
| A.Mg和Al的总质量为9g |
| B.最初20mLNaOH溶液用于中和过量的稀硫酸 |
| C.NaOH溶液物质的量浓度为5mol·L-1 |
| D.生成的氢气在标准状况下的体积为11.2L |
已知:① 向KMnO4晶体滴加浓盐酸,产生黄绿色气体;② 向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色。下列判断正确的为()
| A.上述实验证明氧化性:MnO4->Cl2>Fe3+ |
| B.上述实验中,有一个氧化还原反应 |
| C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
下列表格中各项分类都正确的一组是:( )
 类别 类别选项 |
纯净物 |
混合物 |
电解质 |
非电解质 |
| A |
生理盐水 |
明矾 |
液态KNO3 |
蔗糖 |
| B |
CaO |
海水 |
铜 |
乙醇 |
| C |
胆矾 |
铝合金 |
AgCl |
CO2 |
| D |
氢氧化钠 |
空气 |
Na2SO4溶液 |
食醋 |