(本题共14分)
火力发电厂产生的烟气中含有CO2、CO、SO2等物质,直接排放会对环境造成危害。对烟气中CO2、CO、SO2等物质进行回收利用意义重大。
(1)“湿式吸收法”利用吸收剂与烟气中的SO2发生反应从而脱硫,其中“钠碱法”用NaOH溶液作吸收剂,向100mL0.2mol·L-1的NaOH溶液中通入标准状况下0.448LSO2气体,反应后测得溶液pH<7.则溶液中下列各离子浓度关系正确的是 (填字母序号).
A.c(HSO3-)>c(SO32-)>c(H2SO3)
B.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)
C.c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c(OH-)
(2)CO2是一种温室气体,人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下: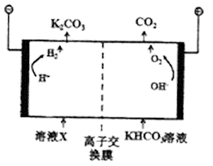
①在阳极区发生的反应包括 和H++HCO3-=CO2↑+H2O.
②简述CO32-在阴极区再生的原理 .
(3)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25℃,101kP下:
① H2(g)+1/2O2(g)=H2O(g) △H1=-242kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H2="-676" kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式 .
(4)已知反应:CO(g)+H2O(g) H2(g)+CO2(g);△H=-41.2kJ/mol.生成的CO2与H2以不同的体积比混合时在合适的条件下反应可制得CH4.
H2(g)+CO2(g);△H=-41.2kJ/mol.生成的CO2与H2以不同的体积比混合时在合适的条件下反应可制得CH4.
①850℃时在一体积为10L的恒容密闭容器中,通入一定量的CO和H2O(g),CO和H2O(g)浓度变化如右图所示。下列说法正确的是 (填序号).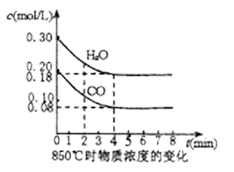
A.达到平衡时,反应体系最终会放出49.44kJ热量
B.第4min时,混合气体的平均相对分子质量不再变化,可判断已达到化学平衡
C.第6min时,若升高温度,反应平衡常数会增大
D.第8min时,若充入CO,会导致v(正)>v(逆),平衡向正反应方向移动
E.0~4min时,CO的平均反应速率为0.030mol/(L•min)
②熔融盐燃科电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。负极反应式为 .为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,为此电池工作时必须有部分A物质参加循环,则A物质的化学式是 .
(1)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液,设由水电离产生的OH-的物质的量浓度分别为A和B,则A和B的关系为 。
(2)在纯碱溶液中滴入酚酞,溶液变红色,若在该溶液中再滴入过量的BaCl2溶液,所观察到的现象是 ,其原因是 。
(3)对于盐AmBn的溶液:
①若为强酸弱碱盐,其水解的离子方程式是 ;
②若为弱酸强碱盐,其水解的离子方程式是 。
(4)已知KSP (Ag2CrO4)=1.12×10-12,将等体积的4×10-3mo1·L-1的AgNO3和4×10-3mo1·L–1K2CrO4混合,________产生Ag2CrO4沉淀(填“能”或“不能”)。
请按要求写出下列反应方程式:
(1)请写出下列溶液水解(或双水解)的离子反应方程式:
①次氯酸钠溶液:
②泡沫灭火器工作原理:
③氯化铁溶液与偏铝酸钾溶液混合:
(2)请写出酸性条件下氢氧燃料电池的电极反应方程式:
负极:
正极:
在恒温、恒容的1L密闭容器中,混合气体X、Y、Z的物质的量n与时间t 的关系如下表所示:X(g)+3Y(g) 2Z(g) △H <0
2Z(g) △H <0
| t/ min n/ mol |
0min |
2min |
4min |
6min |
8min |
| n(X) |
0.2 |
0.15 |
0.1 |
0.1 |
0.05 |
| n(Y) |
0.6 |
0.45 |
0.3 |
0.3 |
0.5 |
| n(Z) |
0 |
0.1 |
0.2 |
0.2 |
0.3 |
(1)第6min末改变了什么条件到达第8分钟的平衡状态: 。
(2)在相同温度下,若1L容器为体积可变的密闭容器,充入0.2molX 、0.6molY,达到平衡时n(Z)="bmol" ,则b 0.2(填“<”、“>”或“=”),平衡时容器的体积V = (用含b的式子表示)
(3)维持温度和压强不变,第6min的平衡体系中再通入0.2molX和0.6molY,达到新平衡时Z的物质的量
(4)维持温度和体积不变,在第6min的平衡体系中再通入0.2molX和0.6molY,达到新平衡时Z的体积分数 (填“增大”、“减小”或“不变”)
在一定温度下,发生反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)。已知该反应在不同温度下的平衡常数如下表:
2Fe(s)+3CO2(g)。已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ |
1000 |
1150 |
1300 |
| 平衡常数 |
64.0 |
50.7 |
42.9 |
请回答下列问题:
(1)该反应的平衡常数表达式K= ,ΔH_____0(填“<”、“>”或“=”)
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10min后达到平衡。求该时间范围内反应的平均反应速率v(CO2)=________,CO的平衡转化率为 。
(3)1000℃时,在(2)的平衡体系中,各加0.5molCO和0.5molCO2,v正 v逆(填“<”、“>”或“=”),平衡向 移动(填“正向”、“逆向”或“不移动”)。
合成氨工业的核心反应是N2(g)+3H2(g) 2NH3(g);反应过程中能量变化如图所示,回答下列问题。
2NH3(g);反应过程中能量变化如图所示,回答下列问题。
(1)该反应的ΔH=____________kJ/mol。
(2)在反应体系中加入催化剂,反应速率增大,E1的变化:E1__________(填“增大”、“减小”或“不变”)。
(3)在500℃、2×107Pa和催化剂条件下,向一密闭容器中充入0.5mol N2和1.5mol H2,充分反应后,放出的热量____________46.2 kJ (填“<”、“>”或“=”) 。
(4)关于该反应的下列说法中,正确的是________(填字母)。
| A.ΔH>0,ΔS>0 | B.ΔH>0,ΔS<0 |
| C.ΔH<0,ΔS>0 | D.ΔH<0,ΔS<0 |
(5)已知298K时白磷、红磷完全燃烧的热化学方程式分别为:
P4(s,白磷)+5O2(g)===P4O10(s)ΔH 1=-2983.2 kJ·mol-1
P(s,红磷)+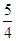 O2(g)===
O2(g)===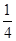 P4O10(s)ΔH 2=-738.5 kJ·mol-1
P4O10(s)ΔH 2=-738.5 kJ·mol-1
则该温度下白磷转化为红磷的热化学方程式为 。