下列化学事实的描述或解释正确的是
| A.Na2SO3溶液中:c(H+)+c(HSO3-)+2c(H2SO3)===c(OH-) |
| B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-==CO32-+H2O |
| C.有些化学反应既属于复分解反应又属于氧化还原反应 |
| D.常温下,将pH=3的HA和PH=11的BOH等体积混合后PH>7,可能生成了弱酸强碱盐 |
下列离子组在指定溶液中能大量共存的是
| A.强酸溶液中:K+、Fe2+、MnO4-、SO2-4 |
| B.滴加石芯试液显红色的溶液中:Fe3+、NH4+、Cl-、SCN- |
| C.既能溶解Al(OH)3又能溶解H2SiO3的溶液中:Na+、CO32-、SO32-、NO3- |
D.常温下 的溶液中:Al3+、NH4+、Cl-、CO32- 的溶液中:Al3+、NH4+、Cl-、CO32- |
下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是
| (I) |
(II) |
|
| A |
将少量浓 氨水滴入Al2(SO)4溶液 氨水滴入Al2(SO)4溶液 |
将少量Al2(SO4)3溶液滴入浓氨水 |
| B |
将少量SO2通入Ba(OH)2溶液 |
将过量SO2通入少量Ba(OH)2溶液 |
| C |
将0.1mol Cl2通入含0.2 molFeBr2的溶液中 |
将0.3mol Cl2 通入含0.2mol FeBr2溶液 通入含0.2mol FeBr2溶液 |
| D |
将过量BaCl2溶液与少量Na2S O4溶液相混合 O4溶液相混合 |
将少量Ba(OH)2溶液与过量MgSO4溶液相混合 |
下列离子方程式书写正确的是
| A.将碳与浓硫酸共热反应后的气体混合物通入过量氢氧化钠溶液中:CO2+SO2+4OH-=SO2-3+CO2-3+2H2O |
| B.向Ca(ClO)2溶液中通入二氧化硫 Ca2++2ClO-+SO2+H2O=2HClO+CaSO3↓ |
| C.向Fe(NO3)3溶液中加入过量的HI溶液 2NO-3+8H++6I-=3I2+2NO↑+4H2O |
D.将等体积等物质的量浓度的NaHCO 3溶液与Ba(OH)2溶液混合:HCO-3+Ba2++OH-=BaCO3↓+H2O 3溶液与Ba(OH)2溶液混合:HCO-3+Ba2++OH-=BaCO3↓+H2O |
下列各组物质依次满足如图所示转化关系的是(图中箭头表示一步转化)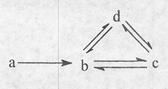
| a |
b |
c |
d |
|
| ① |
Si |
SiO2 |
H2SiO3 |
Na2SiO3 |
| ② |
Al |
AlCl3 |
NaAlO2 |
Al(OH)3 |
| ③ |
Cu |
CuO |
Cu(OH)2 |
CuSO4 |
| ④ |
Na |
NaOH |
Na2CO3 |
NaHCO3 |
| A.①② | B.②③ | C.③④ | D.②④ |
下列实验能达到目的的是
| A.分别加热蒸干灼烧NaAlO2溶液和AlCl3溶液,最终都能得到Al2O3 |
B.在滴有酚酞的 Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡 Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡 |
C.检验Fe2O3中是否含有FeO,用盐酸溶解样品后,滴加高锰 酸钾溶液,观察溶液紫色是否褪色或变浅 酸钾溶液,观察溶液紫色是否褪色或变浅 |
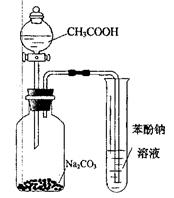
| D.利用图示装置并根据有关实验现象能推知酸性: CH3COOH>H2CO3>C6H2OH |