新型净水剂—高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:①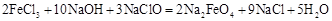
②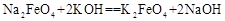 。下列说法不正确的是
。下列说法不正确的是
| A.反应①为氧化还原反应,反应②为复分解反应 |
| B.反应①中氧化产物与还原产物物质的量之比为2:9 |
| C.反应②的产物K2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒 |
| D.若有2mol FeCl3发生反应,转移电子的物质的量为6 mol |
下列关于醋酸钠溶液的说法中正确的是
| A.溶液呈酸性 |
| B.c(H+)= c(CH3COO-)+ c(OH-) |
| C.c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D.c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
25℃时,向V mL pH=a的盐酸中,滴加10V mL pH=b的NaOH溶液,所得溶液中Cl-的物质的量恰好等于Na+的物质的量,则a+b的值是
| A.15 | B.14 | C.13 | D.不能确定 |
室温时,下列混合溶液的pH一定小于7的是
| A.pH=3的盐酸和pH=11的氨水等体积混合 |
| B.pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 |
| C.pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 |
| D.pH=3的硫酸和pH=11的氨水等体积混合 |
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH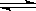 CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
| A.加入少量NaOH固体,平衡向正反应方向移动 |
| B.加水,反应速率增大,平衡向逆反应方向移动 |
| C.滴加少量0.1mol/L HCl溶液,溶液中c(H+)减少 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
常温下某溶液中由水电离产生的[H+]=1×10-5mol·L-1,则下列叙述正确的是
| A.一定是碱溶液 |
| B.一定是酸溶液 |
| C.由水电离出的[OH-]=1×10-9mol·L-1 |
| D.pH值可能为9也可能为5 |