用NA表示阿伏加德罗常数的数值,下列说法中正确的是
| A.在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.3 NA |
| B.22.4L NH3中含有的原子总数为4NA |
| C.1mol单质钠在常温下或点燃条件下与O2完全反应转移的电子数都为NA |
| D.常温条件下,等物质的量浓度的HCl溶液和NaOH溶液混合,溶液pH=7 |
下列物质属于芳香烃,但不是苯的同系物的是
①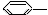 CH3②
CH3②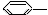 CH=CH2③
CH=CH2③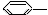 NO2
NO2
④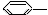 OH ⑤
OH ⑤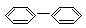 ⑥
⑥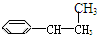
| A.③④ | B.②⑤ | C.①②⑤⑥ | D.②③④⑤⑥ |
分子式为C4H9Cl的同分异构体有
| A.1种 | B.2种 | C.3种 | D.4种 |
由溴乙烷制取乙二醇.依次发生的反应类型是()
| A.取代、加成、水解 |
| B.消去、加成、取代 |
| C.水解、消去、加成 |
| D.消去、水解、取代 |
玻璃器皿上沾有一些用水洗不掉的残留物,其洗涤方法正确的是
①残留在试管内壁上的碘,用酒精洗涤
②盛放过苯酚的试剂瓶中残留的苯酚,用酒精洗涤
③ 做银镜反应后试管壁上银镜,用稀氨水洗涤
④ 沾附在试管内壁上的油脂,用热碱液洗涤
| A.①②④ | B.②③④ | C.①③④ | D.①②③④ |
【改编】某烃与氢气加成后得到2,2-二甲基丁烷,则该烃属于该烯烃的名称是
| A.3,3-二甲基-1-丁炔 | B.2,2-二甲基-2-丁烯 |
| C.2,2-二甲基-1-丁烯 | D.3,3-二甲基-1-丁烯 |