甲、乙、丙、X是中学化学中常见的4种物质,其转化关系符合图。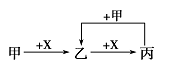
其中甲和X不可能是
| A.甲为Fe,X为Cl2 |
| B.甲为SO2,X为NaOH溶液 |
| C.甲为C,X为O2 |
| D.甲为AlCl3溶液,X为NaOH溶液 |
在胶片冲洗时可用硫代硫酸钠(Na2S2O3)做定影液,与胶片上未曝光的AgBr反应生成可溶性离子Ag(S2O3)23-。该有关过程的离子方程式不合理的是
A.H2S2O3溶液显弱酸性的原因是:H2S2O3 H+ + HS2O3- H+ + HS2O3- |
B.Na2S2O3溶液显碱性的原因是:S2O32-+2 H2O  H2S2O3 + 2OH- H2S2O3 + 2OH- |
C.Na2S2O3和AgBr反应的离子方程式是:2S2O32-+ AgBr  Ag(S2O3)23- + Br- Ag(S2O3)23- + Br- |
| D.定影不能在酸性较强的溶液中进行的原因是:S2O32-+ 2H+=" S↓+" SO2↑+ H2O |
Fe和Mg与H2SO4反应的实验如下:
实验 |
 |
 |
 |
 |
现象 |
Fe表面产生大量无色气泡 |
Fe表面产生气泡后迅速停止 |
Mg表面迅速产生大量气泡 |
Fe表面有大量气泡,Mg表面有少量气泡 |
关于上述实验说法不合理的是
A. I中产生气体的原因是:Fe + 2H+=Fe2++ H2↑
B. 取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体
C. Ⅲ中现象说明Mg在浓H2SO4中没被钝化
D.Ⅳ中现象说明Mg的金属性比Fe强
某兴趣小组为了分析电解硝酸溶液时放电的离子,设计了如图装置进行实验(石墨电极)。电解过程中,X极产生了红棕色气体,则下列说法不合理的是
| A.a极为负极,b极为正极 |
| B.电解时,Y极附近溶液pH降低 |
| C.相同条件下,阴阳两极气体体积比是2:1 |
| D.X极的电极反应式是:2H++ NO3-+ e-=NO2↑ + H2O |
高铁酸钾(K2FeO4)是一种新型非氯高效消毒剂,主要用于饮用水处理。工业上可用如下方法制备:3ClO-+ 2Fe3++ 10OH- = 2FeO42-+ 3Cl-+ 5H2O,下列相关叙述不合理的是
| A.K2FeO4中铁元素的化合价是+6 |
| B.制得1molK2FeO4转移6 mol e- |
| C.K2FeO4做消毒剂的原因是其有强氧化性 |
| D.K2FeO4在消毒杀菌过程中还可以净水 |
活性炭可处理大气污染物NO,反应原理:C(s) + 2NO(g) N2(g) + CO2(g)。T℃时,在2L密闭容器中加入0.100 mol NO和2.030 mol活性炭(无杂质),平衡时活性炭物质的量是2.000mol。下列说法不合理的是
N2(g) + CO2(g)。T℃时,在2L密闭容器中加入0.100 mol NO和2.030 mol活性炭(无杂质),平衡时活性炭物质的量是2.000mol。下列说法不合理的是
| A.该温度下的平衡常数是:K=9/16 |
| B.达到平衡时,NO的转化率是60% |
| C.3min末达到平衡,则v( NO ) = 0.01mol/(L·min) |
| D.升高温度有利于活性炭处理更多的污染物NO |