工业合成氨反应为3H2(g) + N2(g) ⇋2NH3(g) ΔH<0,下列措施能使反应物中活化分子百分数增大的方法是
①增大N2的浓度;②升高温度;③增大压强;④移去NH3;⑤加入催化剂;
| A.①②③ | B.①②③⑤ | C.①②③④⑤ | D.②⑤ |
等质量的CuO和MgO粉末分别溶于相同体积的硝酸中完全溶解,得到的Cu(NO3)2和Mg(NO3)2溶液的浓度分别为a mol·L-1和b mol·L-1,则a与b的关系为( )
| A.a=b | B.a=2b |
| C.2a=b | D.a=5b |
3 g镁铝合金与100 mL稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到无水硫酸盐17.4 g,则原硫酸的物质的量浓度为( )
| A.1 mol·L-1 | B.1.5 mol·L-1 |
| C.2 mol·L-1 | D.2.5 mol·L-1 |
一定量的铜和浓硫酸在加热条件下充分反应,向反应后的溶液中逐滴加入含a mol NaOH的溶液,恰好使反应后的溶液呈中性,则下列叙述错误的是( )
| A.溶液中c(Na+)=2c(SO42-) |
B.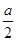 mol>沉淀的物质的量>0 mol>沉淀的物质的量>0 |
C.沉淀的物质的量=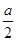 mol mol |
D.原浓硫酸中H2SO4的物质的量>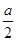 mol mol |
只给出下列甲和乙中对应的量,不能求出物质的量的是( )
| A |
B |
C |
D |
|
| 甲 |
物质的粒子数 |
标准状况下的气体摩尔体积 |
固体的体积 |
溶液中溶质的物质的量浓度 |
| 乙 |
阿伏加德罗常数 |
标准状况下的气体体积 |
固体的密度 |
溶液的体积 |
若20 g密度为ρ g·cm-3的Ca(NO3)2溶液中含有2 g Ca(NO3)2,则溶液中NO3-的物质的量浓度为( )
A. mol·L-1 mol·L-1 |
B. mol·L-1 mol·L-1 |
C.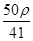 mol·L-1 mol·L-1 |
D.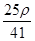 mol·L-1 mol·L-1 |