在0.1mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.通入少量HCl气体,溶液中PH值增大 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
已知芳香烃A、B的结构模型如下图所示,相关叙述正确的是( )
A.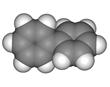 B.
B.
A.A的结构简式为 ,其一氯代物有2种
,其一氯代物有2种
B.A中有两种不同类型的碳碳键
C.B与A互为同系物,通式为CnH4n+2(n为苯环数)
D.与B互为同类别物质的同分异构体共有2种
测定Cu(NO3)2∙nH2O的结晶水含量,下列方案中不可行的是( )
| A.称量样品→加热→冷却→称量CuO |
| B.称量样品→加热→冷却→称量Cu(NO3)2 |
| C.称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量 |
| D.称量样品→加NaOH→过滤→加热→冷却→称量CuO |
下列物质久置于空气中因被氧化而变质且有明显颜色改变的是( )
| A.KMnO4 | B.CuSO4 | C.FeSO4•7H2O | D.C6H5OH |
某溶液中含有大量的Cl一、Br一、I一,若向l L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br一、I一的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,原溶液中Cl一、Br一、I一的物质的量浓度之比为( )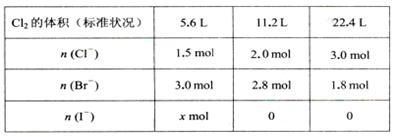
| A.5:15:4 | B.5:12:4 | C.15 : 30 : 8 | D.条件不足,无法计算 |
在含有4 mol HCl和1 mol MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生的沉淀质量m与加入Ba(OH)2物质的量n之间的关系如右图,下列说法正确的是( )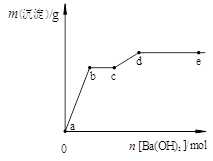
| A.a→b时的沉淀的成分为BaSO4与Mg(OH)2 |
| B.b→c时发生的离子反应为:H+ + OH— → H2O |
| C.c→d时离子的物质的量:Ba2+可能大于Cl— |
| D.d→e时离子的物质的量:Ba2+一定大于OH— |