下列溶液硝酸根离子的物质的量浓度与50ml 1 mol·L-1硝酸铝溶液中硝酸根离子的物质的量浓度相等的是
| A.150 ml、1 mol·L-1硝酸钠溶液 | B.75 ml、2.5 mol·L-1 硝酸钙溶液 |
| C.150 ml、3 mol·L-1硝酸钾溶液 | D.50 ml、3 mol·L-1硝酸镁溶液 |
下列分子中所有原子都在同一条直线上的有机物是( )
| A.C2H2 | B.C2H4 | C.C2H6 | D.CO2 |
化学式为C6H12的某烯烃的所有碳原子都在同一平面上,则该烯烃的结构简式为_______________。
某化合物A的分子式为C5H11Cl,分析数据表明,分子中有两个—CH3、两个—CH2—,一个 和一个—Cl。它的可能结构只有四种。请写出这四种可能的结构简式。
和一个—Cl。它的可能结构只有四种。请写出这四种可能的结构简式。
(1)______________________________________________________。
(2)______________________________________________________。
(3)______________________________________________________。
(4)______________________________________________________。
某烃分子中有一个环和两个碳碳双键,则它的分子式可能是( )
| A.C4H6 | B.C5H6 |
| C.C7H8 | D.C10H16 |
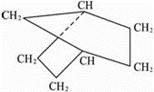
降冰片烷立体结构如下图所示。按键线式(以线示键,每个折点和线端点处表示有一个碳原子,并以氢原子补足四价,C、H不表示出来),写出它的分子式为______________,当它发生一氯取代时,取代位置有_______种。