一定温度下,有可逆反应:2A(g)+2B(g)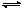 C(g)+3D(g) ΔH<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
C(g)+3D(g) ΔH<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
关于两容器中反应的说法正确的是
| A.甲容器中的反应先达到化学平衡状态 |
| B.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示 |
| C.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量也相同 |
| D.在甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度与乙中物质C的浓度相等 |
下面关于SiO2晶体网状结构的叙述正确的是
| A.存在四面体结构单元,O处于中心,Si处于4个顶角 |
| B.最小的环上,有3个Si原子和3个O原子 |
| C.最小的环上,Si和O原子数之比为1:2 |
| D.最小的环上,有6个Si原子和6个O原子 |
下列判断错误的是
A.沸点: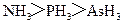 B.熔点:
B.熔点: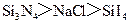
C酸性: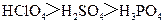 D.碱性:
D.碱性:
已知NaCl的摩尔质量为58.5 g·mol-1,食盐晶体的密度为ρg·cm-3,若下图中Na+与最邻近的Cl-的核间距离为a cm,那么阿伏加德罗常数的值可表示为
A.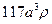 |
B.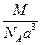 |
C.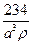 |
D.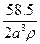 |
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子,其分子结构如图所示,已知断裂1molN—N吸收167kJ热量,生成1molN≡N放出942kJ热量,则下列说法正确的是
| A.N4属于一种新型化合物 |
| B.N4与N2互为同位素 |
C.N4沸点比P4(白磷 )高 )高 |
| D.1molN4气体转变为N2将放出882kJ热量 |
短周期金属元素甲~戊在元素周期表中的相对位置如表所示,下面判断正确的是
| A.原子半径:丙<丁<戊 | B.金属性:甲>丙 |
| C.氢氧化物碱性:丙>丁>戊 | D.最外层电子数:甲>乙 |