下列说法中,错误的是
| A.蔗糖、淀粉、纤维素水解的最终产物都只是葡萄糖 |
| B.误服重金属盐,立即服用牛奶或豆浆可解毒 |
| C.油脂、乙酸乙酯都属于酯类,但不是同系物 |
| D.煤的干馏可以得到苯、甲苯等芳香烃 |
下列有关化学用语使用正确的是
A.氧的原子结构示意图: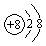 |
B.苯分子的比例模型: |
| C.乙烯的最简式: C2H4 | D.质量数为35的氯原子: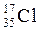 |
在丹麦首都哥本哈根召开的联合国气候变化大会,焦点议题之一是发展“低碳经济”,减少温室气体排放。你认为下列做法中.不能有效减少空气中CO2含量的是
| A.开发利用太阳能、风能、生物能、海洋能等清洁能源 |
| B.使用节能产品,推广节能环保汽车 |
| C.植树造林,增加森林植被面积 |
| D.用脱硫处理的煤代替原煤作燃料 |
对于一定温度和压强下的理想气体,影响其体积大小的主要因素是
| A.分子直径大小 | B.分子间距离大小 |
| C.分子间引力大小 | D.分子数目的多少 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| B.25℃,1.01×105Pa,64gSO2中含有的原子数为3NA |
| C.在常温常压下,11.2L Cl2含有的分子数为0.5NA |
| D.标准状况下,11.2LH2O含有的分子数为0.5NA |