实验证明:若用电解熔融KCl制钾,发现钾熔于熔融KCl中难分离,且电解过程中容易发生爆炸事故等。因而工业不用电解熔融KCl制钾,而用金属钠与KCl共熔置换制钾:
Na(l)+KCl(l)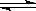 NaCl(l)+K(g) △H>0。 下面是四种物质的熔沸点:
NaCl(l)+K(g) △H>0。 下面是四种物质的熔沸点:
| |
K |
Na |
KCl |
NaCl |
| 熔点/℃ |
63.6 |
97.8 |
770 |
801 |
| 沸点/℃ |
774 |
882.9 |
1500 |
1413 |
根据平衡移动原理,可推知用Na与KCl反应制取金属钾的适宜温度是
A.低于770℃ B.约850℃ C.高于882.9℃ D.1413~1500℃
如图装置可用于收集气体并验证其某些化学性质,正确的是()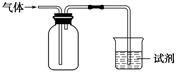
| 选项 |
气体 |
试剂 |
现象 |
结论 |
| A |
NH3 |
酚酞试液 |
溶液变红色 |
NH3的水溶液显碱性 |
| B |
Cl2 |
紫色石蕊试液 |
溶液先变 红后褪色 |
Cl2有酸性和漂白性 |
| C |
C2H2 |
溴水 |
溶液褪色 |
C2H2分子中含碳碳双键 |
| D |
X |
KI淀粉溶液 |
溶液变蓝 |
X可能是Cl2或NO2 |
下列有关物质检验的实验结论正确的是()
| 选项 |
实验操作及现象 |
实验结论 |
| A |
向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
该溶液中一定含有SO42- |
| B |
向某溶液中加入2滴KSCN溶液,溶液不显血红色。再向溶液中加入几滴新制的氯水,溶液变为血红色 |
该溶液中一定含有Fe2+ |
| C |
某气体能使湿润的蓝色石蕊试纸变红 |
该气体水溶液一定显碱性 |
| D |
将少量某有机物滴加到新制氢氧化铜悬浊液中,充分振荡,未见砖红色沉淀生成 |
该有机物不含醛基 |
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是()
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
H2O2、SO2都能使酸性高锰酸钾褪色 |
前者表现出还原性后者表现出漂白性 |
| B |
纯银器表面在空气中渐渐变暗 |
发生了化学腐蚀 |
| C |
SiO2能与氢氟酸及碱反应 |
SiO2是两性氧化物 |
| D |
BaSO4饱和溶液中加入饱和Na2CO3溶液有白色沉淀 |
说明Ksp(BaSO4)大于Ksp(BaCO3) |
用4种溶液进行实验,下表中“试剂和操作”与“现象”对应关系正确的是()
| 选项 |
试剂和操作 |
现象 |
| A |
向AlCl3溶液中滴入过量的氨水 |
溶液先有白色沉淀,后来沉淀消失 |
| B |
向新生成的AgCl浊液中滴入KI溶液,振荡 |
白色沉淀逐渐转化为黄色沉淀 |
| C |
向Ca(ClO)2溶液中先通入CO2,再加入少量品红溶液 |
溶液先变浑浊,通入CO2后品红的红色不褪去 |
| D |
向BaCl2溶液中先通入SO2,再通入过量NO2 |
先生成沉淀,后来沉淀消失 |
下列实验不能达到预期实验目的的是()
| 序号 |
实验内容 |
实验目的 |
| A |
向盛有10滴0.1 mol·L-1 AgNO3溶液的试管中滴加0.1 mol·L-1 NaCl溶液,至不再有沉淀生成,再向其中滴加0.1 mol·L-1 Na2S溶液 |
证明AgCl能转化为溶解度更小的Ag2S |
| B |
向2 mL甲苯中加入3滴酸性KMnO4溶液,振荡;向2 mL苯中加入3滴酸性KMnO4溶液,振荡 |
证明与苯环相连的甲基易被氧化 |
| C |
向Na2SiO3溶液中通入CO2 |
证明碳酸的酸性比硅酸强 |
| D |
向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜悬浊液并加热 |
验证淀粉已水解 |