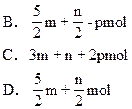一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O(已知:KHC2O4·H2C2O4·2H2O的氧化产物为CO2,H2C2O4为二元弱酸)。若用0.100 0 mol·L-1的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L-1)为
| A.0.008889 | B.0.0800 | C.0.1200 | D.0.2400 |
某烃分子中含有4个原子,14个电子,则此化合物的化学式为
| A.CH4 |
| B.C2H4 |
| C.C2H6 |
| D.C2H2 |
在炼铁制玻璃,制水泥三种工业生产中都需要的原料是
| A.纯碱 |
| B.石灰石 |
| C.石英 |
| D.粘土 |
在水泥厂、冶金厂、硫酸厂常用高压电对气体作用,除去大量烟尘,以减少对空气的污染。这种做法的原因是
| A.胶体凝聚 |
| B.过滤气体 |
| C.胶体电泳 |
| D.丁达尔现象 |
能使蛋白质变性的物质是
①硫酸钾②甲醛③氯酸钾④硝酸汞⑤氯化铵⑥氢氧化钠
| A.②④⑥ |
| B.①③⑤ |
| C.①②③ |
| D.④⑤⑥ |
m molC2H2和n molH2在密闭容器中反应,当其达到平衡时,生成p molC2H4。将平衡混合气体完全燃烧生成CO2和H2O,所需O2的物质的量是
A.3m+nmol