下列表示物质结构的化学用语或模型图正确的是
A.H2O2的电子式: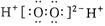 |
B.O2-的结构示意图: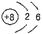 |
| C.二氧化硅的分子式:SiO2 |
D.质子数为8,中子数为10的氧原子: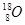 |
常温下,浓度均为0.1 mol/L的三种溶液:①CH3COOH溶液;②NaOH溶液;③CH3COONa溶液。下列说法不正确的是( )
| A.溶液的pH:②>③>① |
| B.水电离出的c(OH-):③>①>② |
| C.②和③等体积混合后的溶液:c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| D.①和②等体积混合后的溶液:c(CH3COOH)+c(CH3COO-)="0.1" mol/L |
常温下,向0.1 mol/L的H2SO4溶液中逐滴加入0.1 mol/L的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示,下列说法中正确的是
( )
| A.a~d溶液的pH:a<b<c<d |
| B.a~d溶液的导电能力:a<b<c<d |
| C.b处溶液的c(H+)与d处溶液的c (OH-)相等 |
| D.c处溶液和d处溶液均呈碱性 |
常温下,将NaHY晶体加入水中溶解,得到0.1 mol/L NaHY溶液,下列叙述正确的是( )
| A.若NaHY溶液的pH=4,该溶液中粒子浓度关系为:c(Na+)>c(HY-)>c(H+)>c(Y2-)>c(H2Y) |
| B.若NaHY的水溶液显碱性,该溶液中粒子浓度关系为:c(Na+)>c(OH-)>c(H+)>c(HY-) |
| C.若溶液中粒子浓度关系为c(H+)+c(H2Y)=c(OH-)+c(Y2-),则NaHY的水溶液一定显碱性 |
| D.将NaHY晶体加入水中一定能促进水的电离 |
25 ℃时,Kw =1.0×10-14;100 ℃时,Kw =5.5×10-13。下列说法正确的是( )
| A.100 ℃时,pH=12的NaOH溶液和pH=2的H2SO4恰好中和,所得溶液的pH=7 |
| B.25 ℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl等体积混合,所得溶液的pH=7 |
| C.25 ℃时,0.2 mol/L NaOH溶液与0.2 mol/L CH3COOH恰好中和,所得溶液的pH="7" |
| D.25 ℃时,pH=12的氨水和pH=2的H2SO4等体积混合,所得溶液的pH>7 |
下列说法正确的是( )
| A.常温下将pH=2的醋酸和pH=12的NaOH溶液等体积混合,所得溶液显碱性 |
| B.已知同温时氢氟酸的电离常数大于亚硝酸的电离常数,则相同温度相同浓度的NaF溶液和NaNO2溶液的碱性:NaF溶液较强 |
| C.将等体积的盐酸和氨水混合,充分反应后所得溶液呈中性,则两溶液的物质的量浓度关系为:c(HCl)<c(NH3·H2O) |
| D.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)= c(CO32-),且c(Mg2+)·c(CO32-)=6.82×10-6 |