下列溶液中各微粒的浓度关系正确的是
A.等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+)=c(K+)=c(Ba2+)
B.将10 mL 0.1 mol·L-1 Na2CO3溶液逐滴滴加到10 mL 0.1 mol·L-1盐酸中:c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-)
C.向NH4HCO3溶液中滴加NaOH溶液至pH=7:c(NH4+)+c(Na+)= c(HCO3-)+c(CO32-)
D.0.2 mol·L-1的某一元弱酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后的溶液:2c(OH一)+c(A一)=2c(H+)+c(HA)
酸碱中和反应的本质是:H+ + OH-= H2O,下列物质间的反应可以用上述离子方程式表示的是
| A.氢氧化铁与硝酸 | B.澄清石灰水与盐酸 |
| C.烧碱与醋酸 | D.氢氧化钡与稀硫酸 |
用NA表示阿伏加德罗常数,下列有关说法正确的是
| A.在常温常压下,11.2LN2含有的分子数小于0.5NA |
| B.标准状况下,2.24LSO3含有的原子数为0.4NA |
| C.将1 L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA |
| D.46gNO2和N2O4混合气体所含氧原子数目有可能为3NA |
下列能达到实验目的的是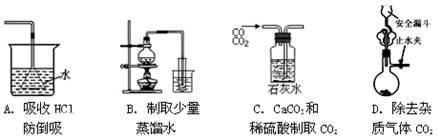
现有三组分散系:①汽油和氯化钠溶液的混合物 ②39%的乙醇溶液 ③氯化钠和单质溴的混合溶液,分离以上各分散系的正确方法依次是
| A.分液、萃取、蒸馏 | B.萃取、蒸馏、分液 |
| C.分液、蒸馏、萃取 | D.蒸馏、萃取、分液 |
下表是某加碘盐包装袋上的部分文字说明:
| 配料 |
氯化钠(NaCl)、碘酸钾(KIO3) |
| 含碘量 |
(35±15)mg·kg—1(以I计) |
| 食用方法 |
菜未烧熟不宜加入加碘盐,菜烧熟后加入加碘盐最佳。 |
根据这一说明某学生作出如下判断,其中正确的是
A.此食盐是纯净物
B.“菜未烧熟不宜加入加碘盐”的原因可能是碘酸钾受热不稳定
C.“加碘食盐”中的“碘”是指碘单质
D.1kg此食盐中含碘酸钾(35±15)mg