电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-===IO+5I-+3H2O,下列说法正确的是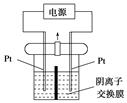
| A.右侧发生的电极反应氧化反应 |
| B.电解结束时,右侧溶液中含有IO3- |
C.电解槽内发生反应的总化学方程式:2KI+2H2O KOH+H2↑+I2 KOH+H2↑+I2 |
| D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应不变 |
下列叙述中能说明金属A肯定比金属B的活泼性强的是 ()
| A.A原子的最外层电子数比B原子的最外层电子数少 |
| B.A原子电子层数比B原子电子层数多 |
| C.1mol A从酸中置换出的H2比1molB从酸中置换的H2多 |
| D.常温时,A能从稀盐酸中置换出氢,而B不能 |
钢铁发生吸氧腐蚀时,正极上发生的电极反应是()






| A.2H++ 2e- ="==" H2↑ | B.Fe2+ + 2e- ="=" Fe |
| C.2H2O + O2 + 4e- ="==" 4OH- | D.Fe3+ + e- ="==" Fe2+ |
如下图所示装置,能够组成原电池且产生电流的是()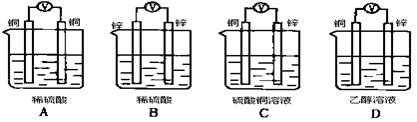
下列热化学方程式或离子方程式中,正确的是()
| A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ·mol-1 |
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) +3H2 (g)  2NH3(g) △H=-38.6kJ· 2NH3(g) △H=-38.6kJ· mol-1 mol-1 |
C.氯化镁溶液与氨水反应: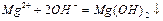 |
| D.氧化铝溶于NaOH溶液:Al2O3 + 2OH- ="=" 2AlO2- + H2O |
下列各组中化合物的性质比较,不正确的是()
| A.酸性:HClO4>HBrO4>HIO4 | B.碱性:NaOH>Mg(OH)2>Al(OH)3 |
| C.稳定性:PH3>H2S> HCl | D.非金属性:F>O>S |