现有Si和Al2O3的固体混合物样品,加入NaOH溶液使混合物完全溶解,所得溶液中c(Na+):c(AlO2—):c(OH—)=6:2:1,则原固体混合物中硅元素与氧元素的质量比为
| A.3:2 | B.3:1 | C.7:8 | D.7:16 |
可逆反应N2+3H2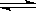 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
| A.3u正(N2)=u正(H2) | B.u正(N2)=u逆(NH3) | C.2u正(H2)=3u逆(NH3) | D.u正(N2)=3u逆(H2) |
在钢铁发生吸氧腐蚀时,正极上发生的电极反应是
| A.2H++2e-=H2 | B.Fe2++2e-=Fe |
| C.2H2O+O2+4e-=4OH- | D.Fe3++e-=Fe2+ |
铅蓄电池的总反应为:PbO2(s)+Pb(s)+2H2SO4(aq)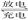 2PbSO4(s)+2H2O(l)关于铅蓄电池的说法正确的是
2PbSO4(s)+2H2O(l)关于铅蓄电池的说法正确的是
| A.在放电时,正极发生的反应是Pb(s)+SO(aq) -2e-=PbSO4(s) |
| B.在放电时,该电池的负极材料是铅板 |
| C.在充电时,电池中硫酸的浓度不断变小 |
| D.在充电时,阳极发生的反应是PbSO4(s)+2e-=Pb(s)+SO(aq) |
室温下,体积相同、pH均为3的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
| A.加水稀释10倍后,两溶液的pH均为4 |
| B.使温度都升高20℃后,两溶液的pH均不变 |
| C.加适量的醋酸钠晶体后,醋酸溶液pH增大,盐酸pH不变 |
| D.加足量的锌充分反应后,醋酸产生的氢气比盐酸多 |
甲酸和乙酸都是弱酸,当它们的浓度均为0.10kJ·mol-1时,甲酸中的c(H+)约为乙酸中c(H+)的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10kJ·mol-1的乙酸,经测定它们的pH从大到小依次为a、乙酸、b。由此可知
| A.a的浓度必小于乙酸的浓度 | B.a的浓度必大于乙酸的浓度 |
| C.b的浓度必小于乙酸的浓度 | D.b的浓度必大于乙酸的浓度 |