下列方程式的书写或描述正确的是( )
| A.用碳酸钠溶液浸泡锅炉水垢:CaSO4+CO32-CaCO3↓+SO42- |
B.热化学方程式C2H2(g)+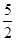 O2(g)2CO2(g)+H2O(g);△H=-1256kJ/mol,表示乙炔的燃烧热为1256kJ/mol O2(g)2CO2(g)+H2O(g);△H=-1256kJ/mol,表示乙炔的燃烧热为1256kJ/mol |
C.铂电极电解MgCl2饱和溶液: |
| D.H+(aq)+OH(aq)H2O(1);△H=-57.3 kJ/mol,表示含1 mol NaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量 |
某烯烃的结构简式为 ,有甲、乙、丙、丁四个同学分别将其命名为:2-甲基4-乙基4-戊烯;2-异丁基-1-丁烯;2,4二甲基-3-乙烯;4-甲基-2-乙基-1-戊烯,下面对4位同学的命名判断正确的是( )
,有甲、乙、丙、丁四个同学分别将其命名为:2-甲基4-乙基4-戊烯;2-异丁基-1-丁烯;2,4二甲基-3-乙烯;4-甲基-2-乙基-1-戊烯,下面对4位同学的命名判断正确的是( )
| A.甲的命名主链选择是错误的 |
| B.乙的命名对主链碳原子的编号是错误的 |
| C.丙的命名主链选择是正确的 |
| D.丁的命名是正确的 |
下列有机物命名正确的是( )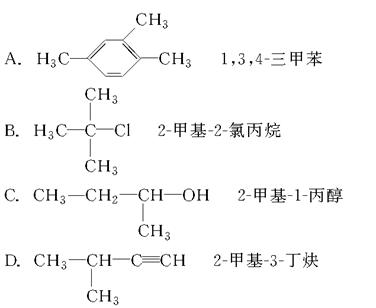
“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,如图是异辛烷的球棍模型,则异辛烷的系统命名为( )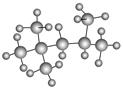
| A.1,1,3,3-四甲基丁烷 |
| B.2-甲基庚烷 |
| C.2,4,4-三甲基戊烷 |
| D.2,2,4-三甲基戊烷 |
某烃经催化加氢后得到2甲基丁烷,该烃不可能是( )
| A.3甲基1丁炔 |
| B.3甲基1丁烯 |
| C.2甲基1丁炔 |
| D.2甲基1丁烯 |
下列各种烃与氢气完全加成后,能生成2,3,3三甲基戊烷的是( )