已知298 K,101 kPa时,2SO2(g)+O2(g) 2SO3(g) ΔH=-197 kJ·mol-1。在相同温度和压强下,向密闭容器中通入2 mol SO2和1 mol O2,达到平衡时,放出热量为Q1,向另一个体积相同的容器中通入1 mol SO2,0.5 mol O2和1 mol SO3,达到平衡时放出热量为Q2,则下列关系正确的是( )
2SO3(g) ΔH=-197 kJ·mol-1。在相同温度和压强下,向密闭容器中通入2 mol SO2和1 mol O2,达到平衡时,放出热量为Q1,向另一个体积相同的容器中通入1 mol SO2,0.5 mol O2和1 mol SO3,达到平衡时放出热量为Q2,则下列关系正确的是( )
| A.Q2<Q1<197 kJ·mol-1 | B.Q2=Q1=197 kJ·mol-1 |
| C.Q1<Q2<197 kJ·mol-1 | D.Q2=Q1<197 kJ·mol-1 |
下列说法中正确的一组是
A.H2和D2互为同位素
B. 和
和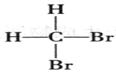 互为同分异构体
互为同分异构体
C.淀粉和纤维素互为同分异构体
D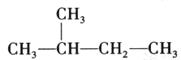 和
和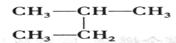 是同一种物质
是同一种物质
下列关于乙烯和聚乙烯的叙述不正确的是
| A.乙烯常温下是气体,为纯净物;聚乙烯常温下是固体,为混合物 |
| B.乙烯的化学性质比聚乙烯活泼 |
| C.取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等 |
| D.乙烯和聚乙烯都能使溴水褪色 |
对可逆反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
| A.达到化学平衡时,4v正(O2)=5v逆(NO) |
| B.若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态 |
| C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 |
| D.化学反应速率关系是2v正(NH3)=3v正(H2O) |
下列化学反应属于取代反应的是
| A.乙烯与酸性高锰酸钾溶液的反应 |
| B.乙烯通入溴的四氯化碳溶液中的反应 |
| C.在浓硫酸作用下,苯在55℃左右与浓硝酸的反应 |
| D.在镍作催化剂、加热的条件下苯与氢气的反应 |
H2在Cl2中燃烧时产生苍白色火焰.在反应过程中,断裂1molH2中的化学键消耗的能量为Q1KJ,断裂1molCl2中的化学键消耗的能量为Q2KJ,形成1molHCl中的化学键释放的能量为Q3KJ.下列关系式正确的是
| A.Q1+Q2>Q3 | B.Q1+Q2>2Q3 | C.Q1+Q2<Q3 | D.Q1+Q2<2Q3 |