下列溶液中各微粒的浓度关系不正确的是( )
| A.0.1mol/L HCOOH溶液中:c(HCOO-)+c(OH-) = c(H+) |
| B.1L 0.1 mol/L CuSO4·(NH4)2SO4·6H2O的溶液中c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) |
| C.0.1mol/LNaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)>c(HCO3-)+c(CO32-)+c(OH-) |
| D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
下列分子式只能表示一种物质的是
| A.C3H7Cl | B.CH2Cl2 | C.C7H8O | D.C2H4O2 |
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是
| A.蒸馏可用于分离提纯液态有机混合物 |
| B.燃烧法是研究确定有机物成分的一种有效方法 |
| C.核磁共振氢普通常用于分析有机物的相对分子质量 |
| D.对有机物分子红外光谱图的研究有助于确定有机物分子中的基团 |
下列变化中,属于物理变化的是
| A.煤干馏 | B.石油的减压分馏 | C.石油裂解 | D.煤液化 |
第一次用无机物制备有机物尿素,开辟人工合成有机物先河的科学家是
| A.瑞典的贝采利乌斯 | B.德国的凯库勒 |
| C.德国的李比希 | D.德国的维勒 |
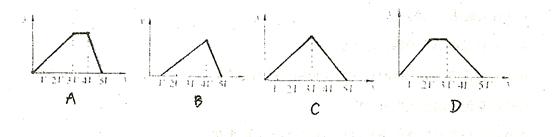
将物质的量相等的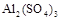 和
和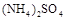 溶于水,形成VL混合溶液,向该混合溶液中逐滴加入某NaOH溶液直至过量。下列各图示中,能正确表示加入NaOH溶液的体积(x)与生成沉淀的物质的量(Y)的关系的是
溶于水,形成VL混合溶液,向该混合溶液中逐滴加入某NaOH溶液直至过量。下列各图示中,能正确表示加入NaOH溶液的体积(x)与生成沉淀的物质的量(Y)的关系的是