聚四氟乙烯( )是不粘锅涂覆物质的主要成分。下列关于聚四氟乙烯的说法,不正确的是( )
)是不粘锅涂覆物质的主要成分。下列关于聚四氟乙烯的说法,不正确的是( )
| A.属于高分子化合物 | B.单体是CF2=CF2 |
| C.可由加聚反应得到 | D.能使高锰酸钾酸性溶液褪色 |
氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2(g)+ O2(g)====H2O(l) ΔH="-285.8" kJ·mol-1
O2(g)====H2O(l) ΔH="-285.8" kJ·mol-1
CO(g)+ O2(g) ====CO2(g) ΔH="-283.0" kJ·mol-1
O2(g) ====CO2(g) ΔH="-283.0" kJ·mol-1
C8H18(l)+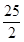 O2(g) ====8CO2(g)+9H2O(l) ΔH="-5" 518 kJ·mol-1
O2(g) ====8CO2(g)+9H2O(l) ΔH="-5" 518 kJ·mol-1
CH4(g)+2O2(g) ====CO2(g)+2H2O(l) ΔH="-890.3" kJ·mol-1
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是()
| A.H2(g) | B.CO(g) | C.C8H18(l) | D.CH4(g) |
在相同温度和压强下,将32 g硫分别在纯氧气中和空气中完全燃烧,令前者放出热量为Q1,后者放出热量为Q2,则关于Q1和Q2的相对大小正确的判断是()
| A.Q1=Q2 | B.Q1>Q2 | C.Q1<Q2 | D.无法判断 |
已知:(1)H2(g)+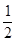 O2(g)====H2O(g) ΔH1=" a" kJ·mol-1
O2(g)====H2O(g) ΔH1=" a" kJ·mol-1
(2)2H2(g)+O2(g)====2H2O(g) ΔH2=" b" kJ·mol-1
(3)H2(g)+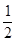 O2(g)====H2O(l) ΔH3=" c" kJ·mol-1
O2(g)====H2O(l) ΔH3=" c" kJ·mol-1
(4)2H2(g)+O2(g)====2H2O(l) ΔH4=" d" kJ·mol-1
下列关系式正确的是()
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
已知化学反应2C(s)+O2(g) 2CO(g),2CO(g)+O2(g)
2CO(g),2CO(g)+O2(g) 2CO2(g)都是放热反应,据此判断,下列说法中不正确的是(其他条件相同)()
2CO2(g)都是放热反应,据此判断,下列说法中不正确的是(其他条件相同)()
| A.12 g碳所具有的能量一定高于28 g CO所具有的能量 |
| B.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量 |
| C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量 |
| D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多 |
在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是()
A.CH3OH(l)+ O2(g)====CO2(g)+2H2O(l) ΔH="+725.8" kJ·mol-1 O2(g)====CO2(g)+2H2O(l) ΔH="+725.8" kJ·mol-1 |
| B.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l) ΔH="-1" 452 kJ·mol-1 |
| C.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l) ΔH="-725.8" kJ·mol-1 |
| D.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l) ΔH="+1" 452 kJ·mol-1 |