室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
| 实验编号 |
起始浓度/(mol·L-1) |
反应后溶液的pH |
|
| c(HA) |
c(KOH) |
||
| ① |
0.1 |
0.1 |
9 |
| ② |
x |
0.2 |
7 |
(1)由实验①写出HA的电离方程式是 。
(2)以下各空均选填“>、<、=”。
实验②反应后的溶液中:c(A-)+c(HA) 0.1mol·L-1
室温下,将pH=3的HA溶液稀释到原体积的10倍后,溶液的pH 4
室温时,向等体积pH=a的盐酸和pH=b的HA溶液中分别加入等量的氢氧化钠后,两溶液均呈中性,则a b
(3)20 mL 0.1 mol/L NaA溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中离子浓度由大到小的顺序是 。
将一定量的NaOH和NaHCO3的混合物放在密闭的容器中加热,充分反应后生成CO2的体积为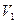 (
(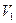 ≠0)。将反应后的固体残渣Y与过量的稀盐酸反应,又生成
≠0)。将反应后的固体残渣Y与过量的稀盐酸反应,又生成 体积的CO2(
体积的CO2(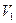 、
、 均为标准状况时的体积)。
均为标准状况时的体积)。
(1)Y的主要成分是_________(写化学式)。
(2)求原混合物中NaOH的NaHCO3的物质的量之比。
(9分)用下列数据求氧原子的电子亲和能
Mg(s) Mg(g)ΔH1="141" kJ·mol-1
Mg(g)ΔH1="141" kJ·mol-1
Mg(g) Mg2+(g)ΔH2="2" 201 kJ·mol-1
Mg2+(g)ΔH2="2" 201 kJ·mol-1 O2
O2 O(g)ΔH3="247" kJ·mol-1
O(g)ΔH3="247" kJ·mol-1
Mg2+(g)+O2-(g) MgO(s)ΔH4="-3" 916 kJ·mol-1
MgO(s)ΔH4="-3" 916 kJ·mol-1
Mg(s)+ O2(g)
O2(g) MgO(s)ΔH5="-602" kJ·mol-1
MgO(s)ΔH5="-602" kJ·mol-1
(14分)Ⅰ.恒温、恒压下,在一个可变容积的密闭容器中发生如下反应:
A(g)+B(g) C(g)
C(g)
(1)若开始时放入1 mol A和1 mol B,达到平衡后,生成a mol C,这时A的物质的量为____ mol。
(2)若开始时放入3 mol A和3 mol B,达到平衡后,生成C的物质的量为__________ mol。
(3)若开始时放入x mol A、2 mol B和1 mol C,达到平衡后,A和C的物质的量分别是y mol和3a mol,则x="__________" mol,y="__________" mol。平衡时,B的物质的量__________(选填一个编号)。
A.大于2 mol B.等于2 mol
C.小于2 mol D.可能大于、等于或小于2 mol
作出此判断的理由是__________。
(4)若在(3)的平衡混合物中再加入3 mol C,待再次达到平衡后,C的物质的量分数是_______。
Ⅱ.若维持温度不变,在一个与I反应前起始体积相同且容积固定的容器中发生上述反应。
(5)开始时放入1 mol A和1 mol B,达到平衡后生成b mol C,将b与(1)小题中的a进行比较____________(选填一个编号)。
A.a<b B.a>b C.a="b" D.不能比较a和b的大小
作出此判断的理由是________________________________________________________。
(12分)向20 mL HCl和H2SO4的混合溶液中逐滴加入0.1 mol·L-1的Ba(OH)2溶液,生成沉淀的质量和溶液的pH与加入的Ba(OH)2溶液体积的关系如图5所示。试完成下列问题: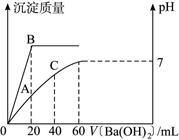
图5
(1)起始时,混合酸中硫酸的物质的量浓度为______________ mol·L-1。
(2)起始时,混合酸中盐酸的物质的量浓度为______________ mol·L-1。
(3)B点表示的沉淀的质量为______________g。
(4)A点表示溶液中的[H+]为______________ mol·L-1,pH为______________。
(5)C点的pH为______________(pH可直接用对数表示)。
某温度下,将一定量密度为1.15 g·cm-3的NaCl溶液用石墨电极通电电解,设NaCl恰好完全反应,且无其他反应发生,得到的溶液中氧元素的质量分数为80%。
(1)求电解后溶液中溶质与溶剂的物质的量之比。
(2)求原NaCl溶液的物质的量浓度。