相同温度下,体积均为1.5 L的两个恒容容器中发生可逆反应:
X2 (g+3Y2(g)  2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
| 容器编号 |
起始时各物质物质的量/mol |
达平衡时体系能量的变化 |
||
| X2 |
Y2 |
XY3 |
||
| ① |
1 |
3 |
0 |
放热46.3 kJ |
| ② |
0.8 |
2.4 |
0.4 |
Q(Q>0) |
下列叙述不正确的是( )
A.容器①中达到平衡时,Y2的转化率为50%
B.Q="27.78" kJ
C.若容器①体积改为1.0 L.则达平衡时放出的热量大于46.3 kJ
D.容器①、②中反应的平衡常数相等,K=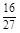
下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是
| A.Na+、Ba2+、Cl-、SO42- | B.MnO4-、K+、I-、H+ |
| C.Ca2+、HCO3-、C1-、K+ | D.H+、Cl-、Na+、CO32- |
某溶液中大量存在如下五种离子:NO3-、SO42-、Fe3+、H+、M,它们的物质的量之比依次为
n(NO3-)∶n(SO42-)∶n(Fe3+)∶n(H+)∶n(M)=2∶3∶1∶3∶1,则M可能是
| A.Al3+ | B.Mg2+ | C.Fe2+ | D.Ba2+ |
下列反应进行分类时,既属于氧化还原反应又属于化合反应的是
A.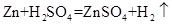 |
B.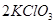   |
C. |
D.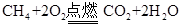 |
等质量的①CH4;②H2;③HCl;④SO2,在标准状况下所占体积由大到小排列的顺序是
| A.②①③④ | B.②①④③ | C.③②④① | D.①④②③ |
在某无色透明的酸性溶液中,能共存的离子组是
| A.Na+ 、K+、SO42-、HCO3- | B.Cu2+、K+、SO42-、NO3- |
| C.Na+、K+、Cl-、NO3- | D.Ba2+、K+、SO42-、Cl- |