水是生命之源,也是人类最宝贵的资源。试用学过的化学知识,回答下列问题:
(1)节约水资源,防止水污染是每个公民应尽的责任和义务。下列做法会造成水体污染的有(填序号) 。
| A.工业废水直接排放 |
| B.生活污水集中处理后排放 |
| C.禁止使用含磷洗衣粉 |
| D.大量使用化肥、农药 |

(2)图A是水通电分解的示意图。写出该反应的化学方程式: 。在实验过程中,试管b中产生的气体是 ,实验室可选用图C制取该气体,该装置中反应的化学方程式为: 。
(3)为除去水中的不溶性杂质,某同学制作了图B所示的简易净水器,其中活性炭的主要作用是 。某些地方的饮用水中含有少量的Ca(HCO3)2,烧水时Ca(HCO3)2发生分解反应,生成难溶性的CaCO3、CO2和一种常见的氧化物。试写出Ca(HCO3)2受热分解的化学方程式 。
(4)下图所示,通过对比实验探究了燃烧需要的条件,此实验中的热水除了起加热的作用,还起 的作用;实验过程中发现,铜片上的红磷一段时间后也燃烧了,原因可能是 。
用数字和化学符号表示。
(1)2个钠离子_____________ ___;
(2)3个硫离子______________ __;
(3)保持氧气的化学性质的微粒____ _______;
(4)F—的结构示意图___ _;
(5)n个铝原子_______ ______
(6)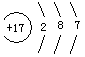 表示的微粒是_______ ___。
表示的微粒是_______ ___。
有两瓶无色液体,一瓶为软水,一瓶为硬水,设计实验区分
| 实验步骤 |
实验现象 |
实验结论 |
如图为电解水实验装置图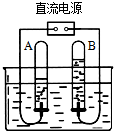
(1) 其中A试管与电极的__________极相连,B试管与电极的__________极相连,A试管中收集到的气体是___________,B试管中的气体检验方法为_________________,
(2)电解水的符号表达式_______________________
(3)该实验得出的结论_________________________
如图是常用的实验装置:

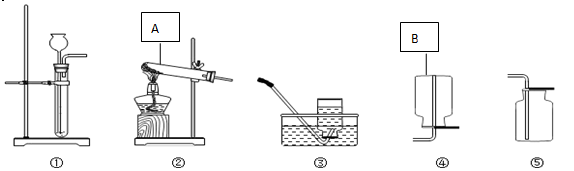
(1)写出仪器标号名称:A ___________ B _____________
(2) 在实验室中用过氧化氢溶液制取氧气,发生装置选择_________(填序号,下同),收集装置应选择______________,反应的文字表达式为___________________
(3)若用高锰酸钾制取氧气,应选择的发生装置为____________,该装置中还缺少______________,该反应的文字表达式_______________________
(4)若氯酸钾的方法制取氧气,应选择的发生装置为_____________,该反应文字表达式______________,该反应为__________反应
将下列物质按要求分类(填序号)
①空气 ② 液氧 ③ 水蒸气 ④ 锰酸钾 ⑤ 红磷 ⑥ 冰水混合物 ⑦自来水 ⑧ 过氧化氢溶液 ⑨ 二氧化硫 ⑩ 氢气
属于混合物的是_____________________
属于纯净物的是__________________
属于单质的是_________________
属于化合物的是__________________
属于氧化物的是______________________