用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A.标准状况下,22.4L H2O含有的分子数为 NA |
| B.常温常压下,1.06g Na2CO3溶于水形成的溶液中含有Na+离子数为0.02 NA |
| C.通常状况下,NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA |
根据相关化学原理,下列判断正确的是()
A.若X是原子晶体,Y是分子晶体,则熔点:X>Y
B.若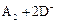 ═
═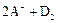 ,则氧化性:D2>A2
,则氧化性:D2>A2
C.若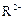 和
和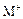 的电子层结构相同,则原子序数:R<M,离子半径:
的电子层结构相同,则原子序数:R<M,离子半径: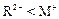
D.若弱酸HA、HB的酸性HA>HB,则溶液的碱性NaA>NaB
下列各组离子能在指定溶液中,可能大量共存的是( )
①无色溶液中:K+、Na+、CO32—、SO42—
②pH=11的溶液中:Na+、Ba2+、AlO2—、ClO—
③水电离出的c(H+) =10—12mol·L—1的溶液中:Mg2+、NH4+、HCO3—、S2—
④加入Al放出H2的溶液中:Cu2+、NH4+、Cl—、NO3—
⑤无色溶液中:K+、Na+、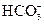 、
、
⑥酸性溶液中:Fe2+、Al3+、NO3—、Cl—
| A.①②④ | B.①②④⑥ | C.①② | D.①②⑤ |
下列关于晶体的说法正确的组合是
①分子晶体常温下都呈液态或气态②在晶体中只要有阴离子就一定有阳离子 ③金刚石、SiO2、NaF、NaCl、H2O晶体的熔点依次降低④分子晶体中只有共价键没有离子键,离子晶体中只有离子键没有共价键⑤氯化铯晶体中每个离子周围均吸引着6个带相反电荷的离子⑥原子晶体中的各相邻原子都以共价键相结合⑦分子晶体中分子间作用力越大,分子越稳定⑧氯化钠熔化时离子键被破坏
| A.②③⑥⑧ | B.①②③⑧ |
| C.③⑤⑥⑦ | D.③⑤⑥⑧ |
下列推断合理的是
| A.明矾[KAl(SO4)2•12H2O]在水中能形成Al(OH)3胶体,Al(OH)3胶体呈电中性 |
| B.金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 |
| C.浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应 |
| D.将SO2通入品红溶液,溶液褪色后加热能恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
 在测定硫酸铜晶体结晶水含量的实验中,下列操作会引起测量结果偏小的是( )
在测定硫酸铜晶体结晶水含量的实验中,下列操作会引起测量结果偏小的是( )
| A.加热前称量时坩埚未完全干燥 | B.加热时间过长,晶体部分变黑 |
| C.加热过程中有少量晶体溅出 | D.粉末未完全变白就停止加热 |