1.52 g铜镁合金完全溶解于50 mL密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL (标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀,下列说法不正确的是( )
| A.该合金中铜与镁的物质的量之比是2∶1 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |
0.1 mol·L-1 Na2CO3和0.1 mol·L-1 NaHCO3溶液的pH,前后两个量的大小关系为( )
| A.大于 | B.等于 | C.小于 | D.不能肯定 |
下列事实不属于盐类水解应用的是()
| A.明矾净水 |
| B.使用热的纯碱溶液去除油污 |
| C.实验室配制FeCl3溶液时加入少量稀盐酸 |
| D.实验室制氢气时加入CuSO4可加快反应速率 |
下列过程或现象与盐类水解无关的是()
| A. | 纯碱溶液去油污 | B. | 铁在潮湿的环境下生锈 |
| C. | 加热氯化铁溶液颜色变深 | D. | 浓硫化钠溶液有臭味 |
上世纪80年代后期人们逐渐认识到,NO在人体内起着多方面的重要生理作用。下列关于NO的说法不正确的是()
| A.NO分子中有极性共价键 |
| B.NO是造成光化学烟雾的因素之一 |
| C.NO是汽车尾气的有害成分之一 |
| D.NO分子所含电子总数为偶数 |
将a L NH3通过灼热的装有铁触媒的硬质玻璃管后,气体体积变为b L(气体体积均在同温同压下测定),该b L气体中NH3的体积分数是()
A.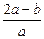 |
B.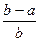 |
C.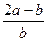 |
D. |