工业上用洗净的废铜作原料来制备硝酸铜。为了节约原料和防止污染环境,宜采取的方法是( )
A. |
B.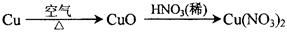 |
C. |
D.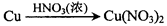 |
在100 mL某混合溶液中,c(HNO3) =" 0.4" mo/lL、c(H2SO4) =" 0.1" mol/L,向其中加入1.92 g Cu粉,微热充分反应后溶液中的c(Cu2+)为()
| A.0.15mol/L | B.0.225mo1/L | C.0.3mo1/L | D.无法计算 |
下列除杂质的方法不可行的是()
| A.用盐酸除去AgCl中少量的Ag2CO3 |
| B.将混合气体通过灼热的铜网除去N2中的少量O2 |
| C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 |
| D.用过量氨水除去Al3+溶液中的少量Fe3+ |
一定条件下,碘单质与砹单质以等物质的量进行反应可得AtI。它与Zn、NH3都能发生反应,化学方程式分别如下:2AtI+2Zn==ZnI2+ZnAt2AtI+2NH3(l)==NH4I+NH2At。
下列关于AtI性质的叙述正确的是()
| A.ZnI2既是氧化产物,又是还原产物 |
| B.ZnAt2既是氧化产物,又是还原产物 |
| C.AtI与液氨反应,AtI既是氧化剂,又是还原剂 |
| D.AtI与液氨反应,是自身氧化还原反应 |
下列各组离子能在指定环境中大量共存的是()
| A.在C(HCO3—)=0.1mol/L的溶液中NH4+、Al3+、Cl-、NO3- |
| B.在由水电离出的C(H+)=1×10-12mol/L的溶液中AlO2-、HCO3-、Na+、SO42- |
| C.在使红色石蕊试纸变蓝的溶液中SO32-、CO32-、Na+、K+ |
| D.pH=1的溶液中Mg2+、Fe2+、NO3-、[Ag(NH3)2]+ |
将0.05 mol NaOH固体分别加入到100 mL下列溶液中,溶液的导电能力变化最小的是()
| A.自来水 | B.0.5 mol·L-1盐酸 |
| C.0.5 mol·L-1醋酸溶液 | D.0.5 mol·L-1KCl溶液 |