下列关于有机物的说法中正确的是( )
①棉花、蚕丝和人造丝的主要成分都是纤维素
②淀粉、油脂、蛋白质在一定条件下都能发生水解
③易溶于汽油、酒精、苯等有机溶剂的物质都是有机化合物
④除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
⑤塑料、橡胶和纤维都是合成高分子材料
⑥石油的分馏、裂化和煤的干馏都是化学变化
| A.①③⑥ | B.②④ | C.①②⑤ | D.④⑥ |
下列各溶液中的离子组能大量共存的是( )
| A.pH=0的溶液中:K+、Fe2+、C1-、NO3- |
| B.强碱性溶液中:Na+、K+、A1O2-、CO32- |
| C.c(H+)=c(OH-)的溶液中:Na+、Ba2+、C1-、SO42- |
| D.使蓝色石蕊试液变红的溶液中:Na+、K+、SO32-、HCO3- |
下列分子中,所有原子不可能共处在同一平面上的是( )
| A.C2H2 | B.HCHO | C.CH2=CHCH3 | D.C6H5OH |
取0.2mol两种气态烃组成的混合气,其质量为3.5g, 则下列说法正确的是( )
| A.一定有乙烯 | B.一定有甲烷 | C.一定没有甲烷 | D.一定有乙烷 |
有一种解热镇痛药的结构简式是: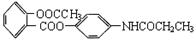 ,当这种物质完全水解时,能够产生的产物有()
,当这种物质完全水解时,能够产生的产物有()
| A.2种 | B.3种 | C.4种 | D.5种 |