A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是
A.A、B、C、D、E
B.E、C、D、B、A
C.B、A、D、C、E
D.C、D、A、B、E
下列电离方程式正确的是()
A.H3PO4 3H++ 3H++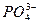 |
B.CaCO3 Ca2++ Ca2++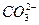 |
C.NaHS Na++H++S2- Na++H++S2- |
D.2H2O H3O++OH- H3O++OH- |
HClO是比H2CO3更弱的酸,反应Cl2+H2O HCl+HClO达到平衡后,要使HClO浓度增大可加入()
HCl+HClO达到平衡后,要使HClO浓度增大可加入()
| A.NaOH | B.HCl | C.CaCO3 | D.H2O |
欲使醋酸溶液中的CH3COO-浓度增大,且不放出气体,可加入的少量固体是()
| A.NaOH | B.碳酸氢钠 | C.醋酸钾 | D.镁 |
对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有 |
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有 |
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有 |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
下列各组物质中,溶液的导电性比反应前明显增强的是()
| A.向亚硫酸钠溶液中加少量液态溴 |
| B.向硝酸银溶液中加入少量氯化氢 |
| C.向氢氧化钠溶液中通入少量氯气 |
| D.向硫化氢饱和溶液中通入适量氯气 |