三明市民新水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
| |
反应前 |
反应后 |
|
| 实验数据 |
烧杯和稀盐酸的质量 |
石灰石样品的质量 |
烧杯和其中混合物的质量 |
| 150 g |
12 g |
157.6 g |
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
(2)求该石灰石中碳酸钙的质量分数。
将4.0gCu – Zn合金粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应。过滤、称量滤液的质量。相关实验数据如下:
| 反应前物质的质量/ g |
反应后物质的质量/ g |
|
| Cu – Zn合金 |
稀硫酸 |
滤液 |
| 4.0 |
10 |
11.26 |
(1)Cu – Zn合金属于材料(“金属”或“有机合成”)
(2)该合金中除Cu、Zn以外的其他成分不与稀硫酸反应,请计算原Cu – Zn合金中Zn的质量分数。写出必要的计算过程。
香椿被称为“树上蔬菜”,是香椿树的嫩芽,它不仅营养丰富,且具有极高的药用价值,如香椿中含有的皂甙具有抗菌、防癌的作用,皂甙的化学式为C27H42O3,请你计算:
(1)皂甙是由种元素组成的;
(2)皂甙中氢元素与氧元素的质量之比是;
(3)皂甙中碳元素的质量分数是(精确到0.1%).
取盐酸溶液60.0g,滴加质量分数26.5%的Na2C03溶液(见下图),溶液pH的变化如右图所示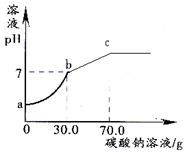
(1)则与盐酸恰好完全反应时碳酸钠溶液的质量为g;
(2)请计算该盐酸溶液恰好完全反应后溶液中的溶质质量分数(写出计算过程,精确到0.1%)。
硫酸铵[(NH4)2SO4]是一种常见的氮肥。请计算(保留小数点后1位):
(1)硫酸铵中氮元素的质量分数为。
(2)100 g质量分数为13.2%的硫酸铵溶液中N元素的质量。
(3)向(2)中溶液加入100 g某浓度的BaCl2溶液,二者恰好完全反应,计算反应后所得溶液中溶质的质量分数。
某化学兴趣小组为了测定铁铜合金中铁的质量分数,取出5g合金样品,将50g稀硫酸分5次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
| 稀硫酸用量 |
10g |
20g |
30g |
40g |
50g |
| 剩余固体质量 |
mg |
3g |
2g |
1g |
1g |
(1)合金样品中铁的质量分数为,
(2)m的值为,
(3)计算加入第一次10g稀硫酸后所得溶液中溶质的的质量分数(结果保留小数点后一位)。