为了防止NO、NO2、N2O4对大气的污染,常用氢氧化钠溶液进行吸收处理,反应的化学方程式2NO2+2NaOH=NaNO3+NaNO2+ H2O,NO2+NO+2NaOH=2NaNO2+H2O。现有由a mol NO、b mol NO2、c mol N2O4组成的混合气体,能被1.0 mol·L-1的氢氧化钠溶液完全吸收,则消耗氢氧化钠溶液的体积最小为
| A.(a+b+c)L | B.2(a+b+c)L | C.(a+b+2c)L | D.3(a+b+c)L |
用下列实验装置进行相应实验,能达到实验目的的是

图1图2图3图4
| A.用图1所示装置,制备并收集少量NO2气体 |
| B.用图2所示装置,除去CO2中的HCl |
| C.用图3所示装置,制备Fe(OH)2并能较长时间观察其颜色 |
| D.用图4所示装置,所示装置制取并收集干燥纯净的NH3 |
下列实验“操作和现象”与“结论”都正确的是
| 操作和现象 |
结论 |
|
| A |
切开金属钠,钠表面的银白色会逐渐变暗 |
Na在空气中会生成Na2O2 |
| B |
向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4溶液颜色基本不变 |
Fe(NO3)2与H2SO4不反应 |
| C |
SO2通入酸性KMnO4溶液,溶液褪色 |
SO2具有漂白性 |
| D |
将充满NO2的试管倒立在水中,试管内液面约上升至试管容积的2/3处;缓慢通入O2,轻轻晃动试管,至液体基本上充满试管 |
从原料的充分利用和减少污染物的排放等方面考虑,该实验对工业生产硝酸有重要启示 |
下表各组物质之间通过一步反应不可以实现如下图所示转化关系的是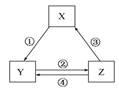
| 选项 |
X |
Y |
Z |
箭头上所标数字的反应条件 |
| A |
CaO |
Ca(OH)2 |
CaCO3 |
①常温加水 |
| B |
AlCl3 |
NaAlO2 |
Al(OH)3 |
②通入CO2 |
| C |
Fe |
FeCl2 |
FeCl3 |
④加入铁粉 |
| D |
Cl2 |
Ca(ClO)2 |
HClO |
③加浓盐酸 |
化学与生活密切相关。下列应用中利用了物质氧化性的是
| A.铁盐制胶体 | B.纯碱去油污 | C.食醋除水垢 | D.漂白粉漂白织物 |