氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂又不是还原剂。下列反应与Cl2+SO2+2H2O=H2SO4+2HCl相比较,水的作用完全相同的是
A.2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
B.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C.2Na+2H2O=2NaOH+H2↑ | D.2Na2O2+2H2O=4NaOH+O2↑ |
下列各组物质的性质比较中,不正确的是:()
| A.金属性强弱:Na >Mg>Al | B.氢化物稳定性:HF > H2O >NH3 |
| C.碱性强弱:KOH>NaOH>LiOH | D.酸性强弱:HIO4 >HBrO4>HClO4 |
下列实验中,可以加快反应速率的是:( )
| A.钠与水反应时,增加水的量 |
| B.锌与稀硫酸反应时,加入少量CuSO4固体 |
| C.用18mol/L的硫酸溶液代替 2mol/L硫酸溶液常温下与铝反应 |
| D.合成氨反应,恒容通入氦气 |
下列说法中正确的是:()
| A.原子及其离子的核外电子层数等于该元素所在的周期数 |
| B.元素周期表中从IIIB族到IIB族 10个纵行的元素都是金属元素 |
| C.第ⅠA族元素的金属性比第ⅡA族元素的金属性强 |
| D.在周期表里,主族元素所在的族序数等于原子核外电子数 |
可逆反应:2NO2(g)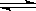 2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是:()
2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是:()
①单位时间内生成n mol O2的同时生成2n mol NO2②单位时间内生成n mol O2的同时生成2n mol NO③用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态
| A.①④ | B.②③⑤ | C.①③④ | D.①②③④⑤ |
下列关于化学键说法正确的是: ( )
| A.构成单质分子的微粒中不一定含有化学键 |
| B.只含有共价键的物质一定是共价化合物 |
| C.NaCl溶于水破坏了离子键,乙醇溶于水破坏了共价键 |
| D.CaCl2 中既有共价键又有离子键 |