将0.2 mol/L的醋酸钠溶液与0.1 mol/L盐酸等体积混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是
| A.c (Cl-)>c (Ac-)>c (HAc)>c (H+) |
| B.c (Ac-)+ c (HAc)= 0.1mol/L |
| C.c (Na+) >c (H+)>c (Ac-)>c (OH-) |
| D.c (Na+)+c (H+)=c (Ac-)+c (Cl-)+c (OH-) |
氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
| A.再通入少量氯气,c(H+)/c(ClO-)减小 |
| B.通入少量SO2,溶液漂白性增强 |
| C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) |
| D.加入少量固体NaOH,溶液的pH会略微增大 |
已知实验室以乙醇为原料来制备乙酸乙酯时,经历了下面三步反应: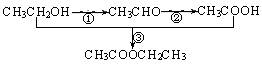 下列说法正确的是:
下列说法正确的是:
| A.乙醇和乙醛能发生氧化反应,乙酸和乙酸乙酯则不能被氧化 |
| B.上述①、②、③的反应类型分别是氧化反应、加成反应和取代反应 |
| C.上述乙醇、乙酸和乙酸乙酯都具有同分异构体 |
| D.工业上可以通过石油分馏的方法获得乙醇 |
下列表述中,不正确的是
| A.用稀盐酸洗涤AgCl沉淀比用水洗涤,损耗AgCl少 |
| B.等体积的 pH均等于3的盐酸和AlCl3溶液中,已电离的水分子数前者一定小于后者 |
| C.高效催化剂可使水分解,同时释放能量 |
| D.明矾用于净水和氯气用于自来水的杀菌消毒,两个反应遵循的化学原理不同 |
环保部门每天通过新闻媒体向社会发布以污染物浓度为标准确定空气质量的信息。这些污染物是()
| A.二氧化硫、氮氧化物、悬浮微粒 | B.二氧化硫、氮氧化物、一氧化碳 |
| C.三氧化硫、氮氧化物、悬浮微粒 | D.稀有气体、氮氧化物、悬浮微粒 |
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,O2-可以在其内部自由通过。其工作原理如图所示。下列关于固体燃料电池的有关说法正确的是()
A.电极b为电池负极,电极反应式为O2+4e- 2O2-
2O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e- 2H++H2O
2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e- 2CO2+2H2O
2CO2+2H2O