钛合金是航天航空工业的重要原料。由钛铁矿(主要成分是TiO2和Fe的氧化物)
制备Ti和绿矾(FeSO4·7H2O)等产品的一种工艺流程示意如下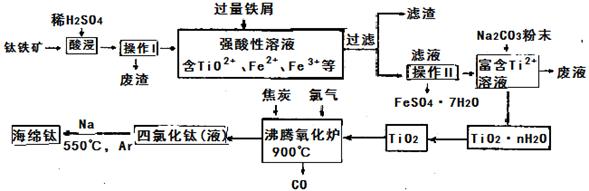
已知:①TiO2+易水解,只能存在于强酸性溶液中 ②TiCl4的熔点-25℃,沸点136.4℃;SiCl4的熔点-68.8℃,沸点57.6℃ 回答下列问题:
(1)TiCl4的晶体类型是 晶体。
(2)TiO2的天然晶体中,最稳定的一种晶体结构如图,其中黑球表示 原子。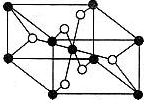
(3)钛铁矿酸浸时,主要成分TiO2反应的离子方程式为 。
(4)操作Ⅱ包含的具体操作方法有 。
(5)废液中溶质的主要成分是 (填化学式)。
(6)沸腾氧化炉中发生反应的化学方程式为 ,
制得的TiCl4液体中常含有少量SiCl4杂质,可采用 方法除去。
(7)若经事先处理后的钛铁矿只含有TiO2和Fe3O4两种氧化物,现有312kg经处理后的钛铁矿,经上述流程后(省去操作Ⅰ)制得了48kg纯净的金属钛。已知在上述流程的强酸性溶液中加过量铁粉时测得转移的电子的物质的量为2a×103mol,则理论上可制得 kgFeSO4·7H2O(假设上述各步反应均完全且各步没有损耗)。
按要求填空:
(1)将等质量的Zn粉分别投入a.10mL0.1mol·L﹣1 HCl和b.10mL 0.1mol·L﹣1醋酸中:
①若Zn不足量,则Zn粉完全反应所需的时间:a b(填“>、<或=”),
②若Zn过量,产生H2的量:a b(填“>、<或=”);
(2)将等质量Zn粉分别投入pH=1体积均为10mL的a.盐酸和b.醋酸中:
①若Zn不足量,则Zn粉完全反应所需的时间:a b(填“>、<或=”),
②若Zn过量,产生H2的量:a b(填“>、<或=”).
请写出下列溶液水解(或双水解)的离子反应方程式:
①次氯酸钠溶液:
②泡沫灭火器工作原理:
③氯化铁溶液与偏铝酸钾溶液混合:
除杂质:所选试剂都填化学式
(1) 除去混入NaCl溶液中少量NaHCO3杂质的试剂是 ,离子方程式为 。
(2) 除去FeCl2溶液中混入的FeCl3溶液杂质用试剂是 ,离子方程式为 。
(3)除去Mg粉中混有的少量Al杂质的试剂是 ,离子方程式为 。
(4)除去NaHCO3溶液中混有的少量Na2CO3 杂质的试剂是 ,离子方程式为 。
化学对人类社会进步和发展的贡献之一是发现和研制了各种材料,例如,金属就是我们生活中不可或缺的重要材料,根据你学过的有关金属的知识,回答下列问题:
(1)铜钱在我国历史上曾经是一种广泛流通的货币,铜常用于制造货币的原因可能是_________(填序号)。
| A.铜的熔点不是太高,易于冶炼,铸造成型 |
| B.铜的性质不活泼,不易被腐蚀 |
| C.我国较早的掌握了湿法冶炼铜的技术 |
| D.自然界有大量的游离态的铜 |
(2)实验室中金属钠保存在________中,钠燃烧的化学方程式为
(3)钢铁制品的使用更为广泛,但是铁制品易生锈,铁锈的主要成分是________(填名称),铁的氧化物常见的还有________、________(填化学式)。
(4)铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但是该氧化膜易被酸碱破坏,若使氧化铝与氢氧化钠溶液作用,反应的化学方程式为:_______________________。
(1)元素的第一电离能:Al Si(填“>”或“<”)。
(2)基态Mn2+的核外电子排布式为 。
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是 。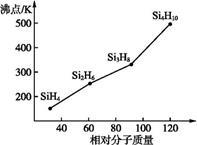
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:
①在Xm-中,硼原子轨道的杂化类型有 ;配位键存在于 原子之间(填原子的数字标号);m= (填数字)。
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有 (填序号)。
A离子键 B共价键 C金属键 D范德华力 E氢键