若NA为阿伏加德罗常数的值。参阅表中数据,下列判断在标准状况下正确的是
| ℃ |
NO2 |
HF |
| 熔点 |
—11.2 |
—83.6 |
| 沸点 |
21.0 |
19.52 |
A.20. 0 gHF中含σ键数目为1.0NA
B.将22.4LNH3溶于1L水中,溶液含有OH-数目为0.1NA
C.6.72 LNO2与水反应后,转移的电子数为0.2NA
D.H2S和SO2各0.l mol反应后,体系中的S原子数目小于0.2NA
有a、b、c、d 4种金属,将a与b用导线连接起来,浸入电解质溶液中,b不易腐蚀;将a、d分别投入等浓度的盐酸中,d比a反应剧烈;将铜浸入b的盐溶液中,无明显变化;如果把铜浸入c的盐溶液中,有金属c析出。据此判断它们的活动性由强到弱的顺序是( )
| A.dcab | B.dabc | C.dbac | D.badc |
如下图所示的装置能够组成原电池且产生电流的是( )
下列烧杯中盛放的都是稀硫酸,在铜电极上能产生气泡的是( )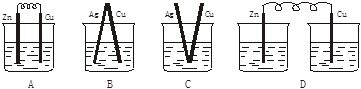
已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧热为-Y kJ/mol,则C与1mol O2反应生成CO时的反应热ΔH为()
| A.-Y kJ/mol | B.-(10X-Y) kJ/mol |
| C.-(5X-0.5Y) kJ/mol | D.+(10X-Y) kJ/mol |
航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化引发高氯酸铵反应,其方程式可表示为: NH4ClO4=N2↑+4H2O+Cl2↑+2O2↑;△H<0 下列对此反应的叙述中错误的是()
| A.上述反应属于分解反应 |
| B.上述反应瞬间产生大量高温气体推动航天飞机飞行 |
| C.反应从能量变化上说,主要是化学能转变为热能和动能 |
| D.在反应中高氯酸铵只能起氧化剂作用 |