工业上向锅炉里注入Na2CO3.溶液浸泡,将水垢中的CaSO4转化为CaCO3而后用盐酸去除。下列叙述不正确的是
| A.温度升高.Na2CO3溶液的Kw和c(OH一)均会增大 |
| B.沉淀转化的离子方程式为CO32- 十CaSO4 = CaCO3 +SO42- |
| C.盐酸溶液中,CaCO3的溶解性大于CaSO4 |
| D.Na2CO3溶液遇CO2后,阴离子浓度均减小 |
下列说法正确的是( )
| A.1 mol葡萄糖能水解生成2 mol CH3CH2OH和2 mol CO2 |
| B.在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 |
| C.油脂不是高分子化合物,1 mol油脂完全水解生成1 mol甘油和3 mol高级脂肪酸 |
| D.欲检验蔗糖水解产物是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2并加热 |
下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述不正确的是( )
A.淀粉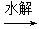 葡萄糖 葡萄糖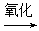 CO2和H2O(释放能量维持生命活动) CO2和H2O(释放能量维持生命活动) |
B.纤维素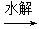 葡萄糖 葡萄糖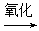 CO2和H2O(释放能量维持生命活动) CO2和H2O(释放能量维持生命活动) |
C.油脂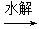 甘油和高级脂肪酸 甘油和高级脂肪酸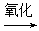 CO2和H2O(释放能量维持生命活动) CO2和H2O(释放能量维持生命活动) |
D.蛋白质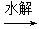 氨基酸 氨基酸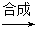 人体所需的蛋白质(人体生长发育) 人体所需的蛋白质(人体生长发育) |
绿色荧光蛋白(green fluorescent protein)简称GFP,这种蛋白质最早是从一种水母中发现的。GFP在蓝光波长范围的光线的激发下,会发出绿色荧光。下列关于GFP的推论正确的是( )
A.组成元素包括C、H、O、N、F、Ne
B.滴加AgNO3溶液可使GFP从溶液中析出,再加蒸馏水后析出物又重新溶解
C.可以通过加聚反应获得
D.在一定条件下可水解生成氨基酸
木糖醇常用做口香糖的甜味剂。木糖醇的结构简式为CH2OH—CHOH—CHOH—CHOH—CH2OH,下列有关木糖醇的说法不正确的是( )
| A.是一种单糖 | B.能发生酯化反应 |
| C.不能发生水解反应 | D.在口腔中不易被氧化 |
某优质甜樱桃中含有一种羟基酸(用M表示),M的碳链结构无支链,分子式为C4H6O5;1.34 g M与足量的碳酸氢钠溶液反应,生成标准状况下的气体0.448 L。M在一定条件下可发生如下转化:M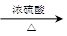 A
A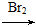 B
B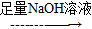 C(M、A、B、C分子中碳原子数目相同)。下列有关说法中不正确的是( )
C(M、A、B、C分子中碳原子数目相同)。下列有关说法中不正确的是( )
A.M的结构简式为HOOC—CHOH—CH2—COOH
B.B的分子式为C4H4O4Br2
C.与M的官能团种类、数量完全相同的同分异构体还有1种
D.C物质不可能溶于水