下列有关推断正确的是
| A.SO3是酸性氧化物,能与NaOH溶液反应 |
| B.Na2O、Na2O2组成元素相同,与CO2反应产物也相同 |
| C.酸酐一定是氧化物,金属氧化物一定是碱性氧化物 |
| D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
某饱和的多元醇3.1 g与足量Na反应生成1.12 L的标准状况下的H2,该多元醇对同温同压下氢气的相对密度为31.0,则多元醇的名称为()
| A.甘油 | B.甲醇 | C.乙醇 | D.乙二醇 |
某有机物的蒸气,完全燃烧时需要三倍于其体积的氧气,产生二倍于其体积的CO2气体,该有机物可能是()
| A.C2H4 |
| B.C2H5OH |
| C.CH3CHO |
| D.CH3COOH |
由—C6H5、—C6H4—、—CH2—、—OH四种原子团(各1个)一起组成属于酚类物质的种类有()
| A.1种 | B.2种 | C.3种 | D.4种 |
由电石跟H2O反应制得有机物A,在催化剂存在时于357 K—369 K发生两分子加成得B。B又与HCl在一定条件下加成得C,C聚合后经硫化处理有下列结构片段: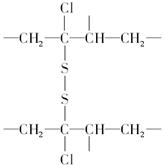
则C的结构简式是()
A.CH2==CH—CH==CH2Cl
B.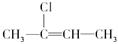
C.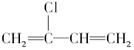
D.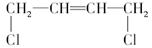
在一密闭容器中,120 ℃时通入a mol CxH4(烃)和b mol O2点火燃烧,生成CO2和水蒸气,等反应完成后恢复至原状态,则反应前后气体体积之比为()
| A.(a+b)∶(2a+b) |
| B.(a+b)∶(a+2b) |
| C.1∶1 |
| D.不能确定 |