已知BaCO3、BaSO4溶度积常数分别为Ksp=5.1×10-9 mol2·L-2,Ksp=1.1×10-10 mol2·L-2,则BaSO4可作钡餐,BaCO3不能作钡餐的主要理由是
| A.BaSO4的溶度积常数比BaCO3的小 |
| B.S没有毒性,C有毒性 |
| C.BaSO4的密度大 |
| D.胃酸能与CO32-结合,生成CO2和H2O,使BaCO3的溶解平衡向右移动,Ba2+浓度增大,造成人体Ba2+中毒 |
X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X、Y和稀硫酸组成原电池时,Y是电池的负极。X、Y、Z三种金属的活动性顺序为
| A.X>Y>Z | B.X>Z>Y | C.Y>X>Z | D.Y>Z>X |
根据下表中所列键能数据,判断下列分子中,最不稳定的分子是
| 化学键 |
H—H |
H—Cl |
H—I |
Cl—Cl |
Br—Br |
| 键能/ kJ/mol |
436 |
431 |
299 |
247 |
193 |
A. HCl B.HBr C.H2 D. Br2
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是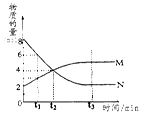
A.反应的化学方程式为:N 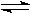 2M 2M |
B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率等于逆反应速率 | D.t3后,若升高温度则反应速率不一定增大 |
某元素原子最外电子层上只有两个电子,该元素
| A.一定是金属元素 | B.一定是ⅡA族元素 |
| C.一定是过渡元素 | D.可能是金属元素也可能不是金属元素 |
以下说法正确的是
| A.C60与金刚石一样属于原子晶体 |
| B.干冰升华破坏了共价键 |
| C.共价化合物中一定不含离子键 |
| D.氯化氢溶于水能电离出H+、Cl—,所以氯化氢是离子化合物 |