可逆反应N2+3H2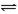 2NH3是一个放热反应。甲、乙是完全相同的容器,甲容器中加入1molN2和3 molH2,一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2 molNH3,达平衡时,吸收的热量为Q2。已知Q2=4Q1,则甲容器中,H2的转化率
2NH3是一个放热反应。甲、乙是完全相同的容器,甲容器中加入1molN2和3 molH2,一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2 molNH3,达平衡时,吸收的热量为Q2。已知Q2=4Q1,则甲容器中,H2的转化率
| A.20% | B.25% | C.75% | D.80% |
240 mL浓度为 0.05 mol·L-1 的Na2SO3溶液 恰好与 200mL浓度为 0.02 mol·L-1的K2X2O7溶液完全反应。已知Na2SO3可被K2X2O7氧化为Na2SO4,则元素X在还原产物中的化合价为
| A.+2 | B.+4 | C.+5 | D.+3 |
在一定条件下,下列微粒的还原性顺序为Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是
| A.2Br-+4H++SO42-===SO2+Br2+2H2O |
| B.2Fe3++SO2+2H2O===2Fe2++SO42-+4H+ |
| C.2Fe2++Cl2===2Fe3++2Cl- |
| D.I2+SO2+2H2O===4H++SO42-+2I- |
能正确表示下列反应的离子方程式
| A.NH4HCO3溶于过量的浓KOH溶液中:NH4+HCO3-+2OH-=CO32-+NH3↑+2H2O |
| B.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| C.向FeBr2溶液中通入少量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| D.醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O |
下列各组离子在指定溶液中能大量共存的是
| A.pH=11的溶液中:CO32-、Na+、AlO2-NO3-[ |
| B.无色溶液中:K+、Na+、MnO4-、SO42- |
| C.加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+ |
| D.酸性溶液中:Fe2+、Al3+、NO3-、Cl- |
水溶液中能大量共存的一组离子是
| A.Na+、Al3+、Cl﹣、CO32﹣ | B.H+、Na+、Fe2+、MnO4﹣ |
| C.K+、Ca2+、Cl﹣、NO3﹣ | D.K+、NH4+、OH﹣、SO42﹣ |