在可逆反应2A(g)+3B(g) xC(g)+D(g)中,已知:反应开始加入的物质只有A、B,起始浓度A为5 mol·L-1,B为3 mol·L-1,前2 min C的平均反应速率为0.5 mol·L-1·min-1。2 min末,测得D的浓度为0.5 mol·L-1。则关于此反应的下列说法中正确的是
xC(g)+D(g)中,已知:反应开始加入的物质只有A、B,起始浓度A为5 mol·L-1,B为3 mol·L-1,前2 min C的平均反应速率为0.5 mol·L-1·min-1。2 min末,测得D的浓度为0.5 mol·L-1。则关于此反应的下列说法中正确的是
A.2 min末时A和B的浓度之比为5∶3
B.x=1
C.2 min末时B的浓度为1.5 mol·L-1
D.前2 min,A的消耗浓度为0.5 mol·L-1
某学生的实验报告所列出的下列数据中合理的是()
| A.用1mol的醋酸溶液和1.01mol的氢氧化钠溶液做中和热实验测得中和热的数值为57.3KJ/mol |
| B.通过实验得知在常温常压下,12g固体C和32g气体O2所具有的总能量一定大于44g气体CO2所具有的总能量 |
| C.取106gNa2CO3固体溶于1L水所得的溶液浓度为1mol·L—1 |
| D.用10mL的量筒量取8.05mL浓硫酸 |
以下说法中正确的是()
| A.所有△H<0的反应均是自发反应 | B.自发进行的反应一定能迅速进行 |
| C.冰在室温下自动熔化成水,是熵增的过程 | D.高锰酸钾加热分解是一个熵减小的过程 |
将0.4 g NaOH和1.06 g Na2CO3混合并配制成溶液,向溶液中逐滴加入0.1 mol·L-1的盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是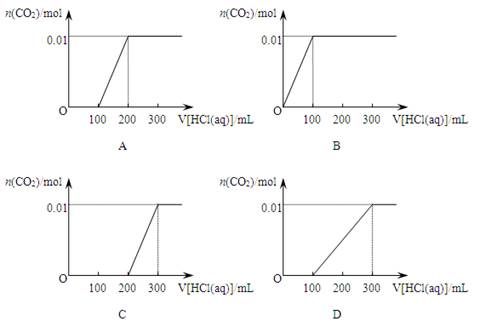
下列关于焰色反应说法不正确的是
| A.某些金属的单质和化合物在火焰上灼烧时都能显现特殊的颜色,因此焰色反应是元素的性质。 |
| B.钾的焰色为紫色,必须通过蓝色钴玻璃才能观察到。 |
| C.焰色反应是物理过程,但也可能伴随着化学变化。 |
| D.烟花能显现出五颜六色,与烟花中含有某些金属元素的盐类有关。 |
下列关于金属的描述不正确的是
| A.金属单质都有还原性 |
| B.镁、铝虽然还原性较强,但可以直接置于空气中保存,是因为表面能形成致密的氧化膜,保护了内层的金属 |
| C.铝箔在酒精灯上加热后熔化但不滴落,是因为表面形成的Al2O3层熔点很高 |
| D.钠和镁可以剧烈地燃烧,铝和铁则不能燃烧 |