25℃时,水中存在电离平衡:H2O  H++OH- △H>0。下列叙述正确的是
H++OH- △H>0。下列叙述正确的是
| A.将水加热,KW增大,pH不变 |
| B.向水中加入少量NaHSO4固体,c(H+)增大,KW不变 |
| C.向水中加入少量NaOH固体,平衡逆向移动,c(OH-)降低 |
| D.向水中加入少量NH4Cl固体,平衡正向移动,c(OH-)增大 |
常温下,把pH=2的H2SO4和pH=11的NaOH溶液混和,若使混和液pH=7,则酸与碱溶液的体积比是
| A.10:1 | B.1:10 | C.1:2 | D.2:1 |
某原电池的电池反应为:Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是
| A.铜片、铁片、FeCl3溶液组成的原电池 |
| B.石墨、铁片、Fe(NO3)3溶液组成的原电池 |
| C.铁片、锌片、Fe2(SO4)3溶液组成的原电池 |
| D.铜片、铁片、Fe(NO3)3溶液组成的原电池 |
在298K、100kPa时,已知:①、2H2O(g)=O2(g)+2H2(g) ΔH1
②、Cl2(g)+H2 (g)=2HCl(g) ΔH2
③、2Cl2(g)+2 H2O (g)=4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是
| A.ΔH3=ΔH1+2ΔH2 | B.ΔH3=ΔH1+ΔH2 |
| C.ΔH3=ΔH1-2ΔH2 | D.ΔH3=ΔH1-ΔH2 |
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
| A.加入少量NaOH固体,平衡向逆反应方向移动 |
| B.升高温度,平衡向正反应方向移动 |
| C.加入水稀释,溶液中c(H+)一定增大 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
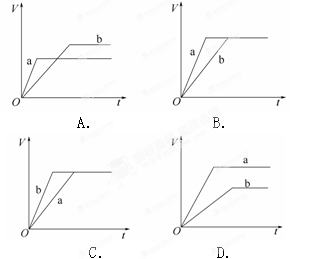
将等质量的两份锌粉a、b分别加入过量的稀硫酸。同时向a中加入少量CuSO4溶液。图中产生H2的体积V L与时间t min的关系正确的是