某同学对一无色透明溶液进行分析得出该溶液中含有下列某组离子,你认为该组离子应该是
| A.Al3+、NO3―、K+、SO42ˉ | B.Ca2+、H+、CO32ˉ、AlO2― |
| C.OHˉ、SO42ˉ、NH4+、Al3+ | D.Fe3+、Mg2+、NO3ˉ、Clˉ |
在a、b、c、d四个集气瓶中分别盛有H2、Cl2、HCl、HBr中的任一种气体,若将a和d两瓶气体混合后见光爆炸;若将a和b两瓶气体混合后,瓶壁上出现暗红色液滴,则a、b、c、d四个集气瓶中分别盛放的气体是()
| A.Cl2、H2、HCl、HBr | B.Cl2、HCl、HBr、H2 |
| C.Cl2、HBr、H2、HCl | D.Cl2、HBr、HCl、H2 |
下列关于碱金属元素和卤素的说法中,错误的是()
| A.随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大 |
| B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强 |
| C.钠与水的反应不如钾与水的反应剧烈 |
| D.溴单质与水的反应比氯单质与水的反应更剧烈 |
下列说法正确的是()
| A.F、Cl、Br的最外层电子数都是7,次外层电子数都是8 |
| B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律 |
| C.卤素按F、Cl、Br、I的顺序其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起主要作用 |
| D.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl4 |
已知钡的活动性介于钠和钾之间,下列叙述正确的是()
| A.钡与水反应不如钠与水反应剧烈 |
| B.钡可以从KCl溶液中置换出钾 |
| C.氧化性:K+>Ba2+>Na+ |
| D.碱性:KOH>Ba(OH)2>NaOH |
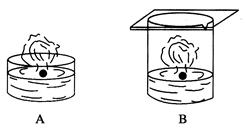
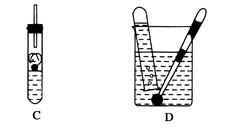
下列四种演示金属钾与水反应的实验装置,正确的是()