NA表示阿伏加德罗常数的值。下列判断中,正确的是
| A.H2O2溶液中加入MnO2可制得O2,产生2.24L(标况)O2,转移0.4NA个电子 |
| B.SO2和CO2都属于酸性氧化物,Na2O和A12O3都属于碱性氧化物 |
| C.在氯化铵水溶液中,既存在水解平衡,又存在电离平衡 |
| D.O2在放电的条件下生成O3属于化学变化,电解质溶液导电属于物理变化 |
某岛屿引入外来物种野兔,研究人员调查了30年间野兔种群数量的变化,并据此绘制了λ值变化曲线。以下叙述正确的是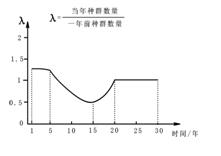
| A.第1年至第5年间野兔种群数量保持相对稳定 |
| B.第5年起野兔种群数量开始下降 |
| C.第15年至第20年间野兔种群数量呈“J”型增长 |
| D.第20年到第30年间野兔种群数量的增长率为0 |
下列对图中有关的生物学意义描述正确的是: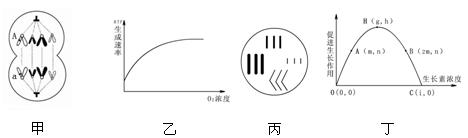
| A.甲图细胞来源于某二倍体生物,其中可能发生了基因突变,也可能发生了交叉互换 |
| B.乙图可以表示ATP生成速率与O2浓度的关系 |
| C.丙图所示的细胞是三倍体 |
| D.若测得胚芽鞘向光一侧与背光一侧生长素含量之比为1:2,则据丁图推测胚芽鞘尖端背光一侧的生长素的浓度范围是m<x<2m |
同位素标记法是用放射性同位素标记的化合物追踪物质的运行和变化规律,从而揭示生命的机理。下列对一些重大科学发现过程中应用同位素标记法的叙述不正确的是
| A.鲁宾和卡门利用18O标记H2O和CO2,证明光合作用释放的氧气来自于水 |
| B.卡尔文利用14C标记CO2,探明光合作用中有机物的转化途径 |
| C.科学家在豚鼠的胰腺细胞中注射3H标记的亮氨酸,追踪分泌蛋白的合成和运输过程 |
| D.赫尔希和蔡斯利用分别含35S和32P的培养基培养噬菌体,实现噬菌体的标记,进而证明DNA是遗传物质 |
下列有关变异的叙述,正确的是
| A.发生在体细胞内的基因突变是不能遗传给后代的,因而属于不可遗传的变异 |
| B.所有的单倍体都不可育 |
| C.原核细胞和真核细胞均可能发生基因突变,但没有细胞结构的病毒则不能发生 |
| D.由配子直接发育而来的个体,不论体细胞中含有几个染色体组都叫单倍体 |
HIV能通过细胞表面的CD4(一种受体蛋白)识别T细胞(如图甲),如果给AIDS患者大量注射用CD4修饰过的红细胞,红细胞也会被HIV识别、入侵(如图乙)。因HIV在红细胞内无法增殖,红细胞成为HIV的“陷阱细胞”。这为治疗AIDS提供了新的思路。据材料分析,下列叙述不正确的是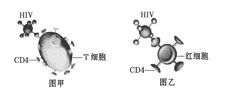
| A.CD4与双缩脲试剂反应呈紫色 |
| B.HIV通过攻击红细胞可使人的免疫功能全部丧失 |
| C.红细胞可作为“陷阱细胞”与其结构有关 |
| D.入侵到红细胞的HIV随红细胞凋亡后可被免疫系统清除 |