已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) △H1 2H2(g)+O2(g)=2H2O(g) △H2
C(s)+O2(g)=CO2(g) △H3 H2O(g)=H2O(l) △H4
则反应4 C3H5(ONO2)3(l)=12CO2(g)+10H2O(l)+O2(g)+6N2(g)的△H为
| A.12△H3+5△H2-2△H1+10△H4 | B.2△H1-5△H2-12△H3+10△H4 |
| C.12△H3-5△H2-2△H1+10△H4 | D.△H1-5△H2-12△H3+10△H4 |
某溶液中存在XO3―,且X为短周期元素,则一定能在该溶液中大量共存的离子组是
| A.Na+、H+、SO42―、I― | B.Na+、Ca2+、CO32―、Al3+ |
| C.Na+、K+、Fe2+、H+ | D.K+、SO42―、Cl―、CO32― |
1966年,范克等人提出用H2O、SO2和I2为原料进行热化学循环制氢法:
2H2O(l)+SO2(g)+I2(s) H2SO4(aq)+2HI(g); H2SO4(aq)
H2SO4(aq)+2HI(g); H2SO4(aq)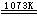 H2O(l)+ SO2(g)+
H2O(l)+ SO2(g)+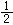 O2(g);
O2(g);
2HI(g) 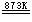 H2(g)+I2(g)。从理论上讲,该循环中,a mol原料水能制得氢气
H2(g)+I2(g)。从理论上讲,该循环中,a mol原料水能制得氢气
| A.a mol | B.0.5a mol | C.0.25a mol | D.2a mol |
在密闭容器中,将1.0 mol CO与1.0 mol H2O混合加热到800℃,发生下列反应:CO(g)+H2O(g) CO2(g)+H2(g)。一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是
CO2(g)+H2(g)。一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是
| A.800℃下,该反应的化学平衡常数为0.25 |
| B.427℃时该反应的平衡常数为9.4,则该反应的△H<0 |
| C.同温下,若继续向该平衡体系中通入1.0 mol的H2O(g),则平衡时CO转化率为66.7% |
| D.同温下,若继续向该平衡体系中通入1.0 mol的CO(g),则平衡时CO物质的量分数为33.3% |
某研究小组用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法错误的是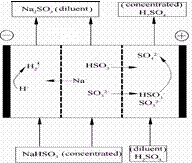
| A.阳极区酸性增强 |
| B.阴极区电极反应式为:2H++2e—=H2↑ |
| C.diluent和concentrated的中文含义为浓缩的、稀释的 |
| D.该过程中的副产品主要为H2SO4 |
已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
1.8×l0_5 |
4.9×l0_10 |
K1=4.3×l0_7 K2=5.6×l0_11 |
则下列有关说法正确的是
| A.等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B.a mol·L—1 HCN溶液与b mol·L—1 NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b |
| C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小 |
| D.NaHCO3和Na2CO3混合溶液中,一定存在c(Na+)+ c(H+)=c(OH-)+ c(HCO3-) +2c(CO32-) |