关于下列各装置图的叙述中,不正确的是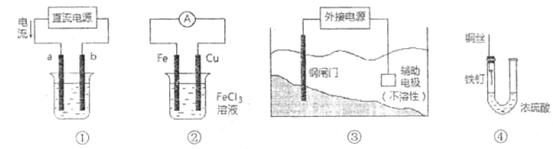
A.用装置①精炼铜,则a极为粗铜,电解质溶液为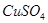 溶液 溶液 |
B.装置②的总反应是: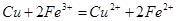 |
| C.装置③中钢闸门应与外接电源的负极相连 |
D.装置④中的铁钉几乎 没被腐蚀 没被腐蚀 |
根据已知条件,对物质的性质强弱判断不正确的是
A.已知 ,说明非金属性:碳>硅 ,说明非金属性:碳>硅 |
B.已知相同条件下气态氢化物的稳定性 ,说明还原性: ,说明还原性: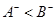 |
C.已知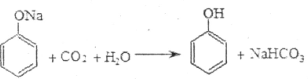 ,说明酸性:碳酸>苯酚 ,说明酸性:碳酸>苯酚 |
D.已知相同物质的量浓度的 两溶液中 两溶液中 ,说明碱性: ,说明碱性: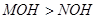 |
甲、乙两种物质的溶解度曲线如下图所示,下列说法一定正确的是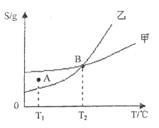
A.A点表示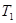 ℃时甲的 ℃时甲的 溶液已知饱和, 溶液已知饱和, 乙的溶液未饱和 乙的溶液未饱和 |
B.B点表示 ℃时甲、乙两物质的溶液均饱和,且两溶液的物质的量浓度相等 ℃时甲、乙两物质的溶液均饱和,且两溶液的物质的量浓度相等 |
C.B点表示 ℃时甲、乙两物质溶液的溶质的质量分数相等 ℃时甲、乙两物质溶液的溶质的质量分数相等 |
D.B点表示 ℃时甲、乙两物质溶液的密度相等 ℃时甲、乙两物质溶液的密度相等 |
下列离子方程式书写正确的是
A.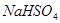 溶液与 溶液与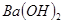 溶液混合后溶液呈中性: 溶液混合后溶液呈中性: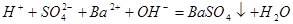  |
B.标准状况下将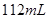 氯气通入 氯气通入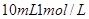 的溴化亚铁溶液中: 的溴化亚铁溶液中: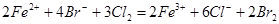 |
C.用硫化亚铁与稀硝酸反应制 气体: 气体: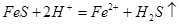 |
|
D.用 澄清石灰水中加入过量的碳酸氢钠溶液: 澄清石灰水中加入过量的碳酸氢钠溶液: |

红磷(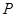 )和
)和 发生反应生成
发生反应生成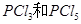 ,反应过程和能量关系如下图所示,图中的△H表示生成
,反应过程和能量关系如下图所示,图中的△H表示生成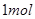 产物的数据。已知
产物的数据。已知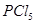 分解生成
分解生成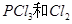 ,该分解反应是可逆反应,下列说法正确的是
,该分解反应是可逆反应,下列说法正确的是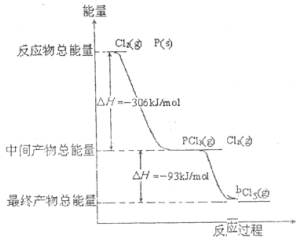
A.其他条件不变,升高温度有利于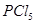 的生成 的生成 |
B.反应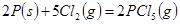 对应的反应热 对应的反应热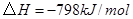 |
C.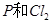 反应生成 反应生成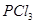 的热化学方程式为: 的热化学方程式为: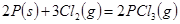 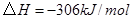 |
D.其他条件不变,对于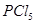 分解生成 分解生成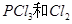 的反应,增大压强, 的反应,增大压强,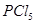 的转化率减小,平衡常数K减小 的转化率减小,平衡常数K减小 |